- Рекоммендации АФР online
- Ретикулярные вены и телеангиэктазии нижних конечностей. АФР 1_2024
Рекомендации АФР online
Поиск по разделу
Ретикулярные вены и телеангиэктазии нижних конечностей. Клинические рекомендации
АФР ID: 1_2024
Рекомендации утверждены голосованием Исполнительного Совета АФР (голосование ИС №62 28.01.2024). Текст рекомендаций направлен на утверждение в МЗ РФ и может быть обновлен по результатам рецензирования и утверждения.
ID минздрава: на утверждении
МКБ 10: I86.2, I86.3, I87.1
Разаботчик: Ассоциация флебологов России;
При участии: Ассоциация сердечно-сосудистых хирургов России, Российское общество хирургов, Российское общество ангиологов и сосудистых хирургов
Текст в pdf
Скачать текст рекомендаций в формате pdf
Список сокращений
АФР – ассоциация флебологов России
БПВ – большая подкожная вена
ДСВНК - дуплексное сканирование вен нижних конечностей
МПВ – малая подкожная вена
НПВС – нестероидные противовоспалительные средства
РВ – ретикулярная вена, ретикулярные вены
СПС – сафено-поплитеальное соустье
СФС – сафено-феморальное соустье
ТАЭ – телеангиэктазия
ХЗВ – хронические заболевания вен
ЧЛК – чрескожная лазерная коагуляция
ХВН – хроническая венозная недостаточность
CEAP (Clinical Etiology Anatomy Pathophysiology) – международная классификация хронических заболеваний вен нижних конечностей
Nd:YAG – лазер на иттрий-алюминевом гранате с неодимом
PDL – лазеры на красителях
Термины и определения
Варикозное расширение подкожных вен (варикозная трансформация подкожных вен) - подкожные расширенные вены диаметром более 3 мм в положении стоя. Обычно имеют узловатый (мешковидный) и/или извитой (змеевидный) вид.
Вторичные телеангиэктазии – потенциально обратимое осложнение устранения внутрикожных и подкожных вен, проявляющиеся в возникновении новых телеангиэктазий размерами менее 0,2 мм в диаметре в местах проведенного лечения. Синонимы: мэттинг, телеангиэктатический мэттинг. Англоязычный термин: telangiectatic matting.
Гиперпигментация – потенциально обратимое осложнение устранения внутрикожных и подкожных вен, проявляющиеся во внутрикожном отложении гемосидерина в местах проведенной микросклеротерапии или чрескожной лазерной коагуляции
Дуплексное сканирование вен нижних конечностей (код медицинской услуги A04.12.006) - метод ультразвукового исследования вен, при котором, в случае необходимости, возможно одновременное использование двух или трех режимов сканирования. Является одним из видов ультразвукового исследования крупных кровеносных сосудов (A04.12). Ретикулярные вены – расширенные и извитые подкожные вены 1-3 мм в диаметре.
Склеротерапия (склерооблитерация) – метод устранения внутрикожных и подкожных вен, заключающийся во внутривенной инъекции химического препарата (склерозанта) с целью разрушения внутренней стенки сосуда и последующим развитием внутрисосудистого фиброза. Микросклеротерапией принято называть склеротерапию телеангиэктазий, однако иногда этот термин применяют для обозначения склеротерапии и телеангиэктазий, и ретикулярных вен.
Телеангиэктазии (телеангиэктазы, телангиэктазы) – расширенные внутрикожные вены менее 1 мм в диаметре.
Флебэктатическая корона - веерообразно расположенные множественные телангиэктазы на медиальной или латеральной поверхности стопы и голеностопного сустава
Чрескожная лазерная коагуляция (медицинские услуги A22.01.004 Лазерная коагуляция телеангиоэктазий, A22.12.003 Лазерная коагуляция вен нижних конечностей) – метод устранения внутрикожных и подкожных вен, заключающийся в избирательном поглощении тепловой энергии лазерного излучения гемоглобином стенки вены с последующим ее нагревом и фиброзом.
1. Краткая информация по заболеванию или состоянию (группе заболеваний или состояний)
1.0. Определение заболевания или состояния (группы заболеваний или состояний)
В настоящих рекомендация рассматривается класс хронических заболеваний вен нижних конечностей, образуемый наличием ретикулярных вен (РВ) и телеангиэктазий (ТАЭ) и классифицируемый в международной классификации CEAP как С1
1.1. Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Единых взглядов на причины и факторы развития ретикулярных вен и телеангиэктазий нижних конечностей к настоящему времени нет.
1.2. Эпидемиоогия заболевания или состояния (группы заболеваний или состояний)
Официальных статистических данных о распространенности ретикулярных вен и телеангиэктазий среди населения Российской Федерации нет. По данным единичных российских популяционных исследований распространенность класса С1 среди взрослых составляет 30% [1]
1.3. Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
Другие поражения вен (I87):
I87.8 – Другие уточненные поражения вен
1.4. Классификация заболевания или состояния (группы заболеваний или состояний)
1.4.1. Классификация CEAP.
При формулировке диагноза по поводу хронических заболеваний вен нижних конечностей рекомендуется использовать классификацию CEAP. РВ и ТАЭ нижних конечностей являются самостоятельным классом хронических заболеваний вен нижних конечностей, обозначаемым как класс С1 в международной классификации CEAP.
Классификация CEAP отвечает как запросам повседневной практики, так и соответствует нуждам исследовательской работы в области флебологии. Классификация СЕАР учитывает клинические проявления (C – clinic), этиологию (E – etiology), анатомическую локализацию (A – anatomy) и патогенез (P – pathogenesis) заболевания. Она рекомендована к использованию всеми ведущими профессиональными ассоциациями по флебологии [2-10]. Классификация CEAP приведена в таб. 1.
Таблица 1. Международная классификация хронических заболеваний вен нижних конечностей (CEAP) [8]
|
Параметр |
Описание |
|
С класс |
Клинические проявления |
|
С0 |
Нет видимых признаков |
|
С1 |
Телеангиэктазии и ретикулярные вены |
|
С2 |
Варикозное расширение вен |
|
С2r |
Рецидив варикозного расширения вен |
|
С3 |
Венозный отек |
|
С4а |
Пигментация и экзема |
|
С4b |
Липодерматосклероз или белая атрофия кожи |
|
С4с |
Флебэктатическая корона |
|
С5 |
Зажившая венозная язва |
|
С6 |
Открытая венозная язва |
|
С6r |
Открытая рецидивная венозная язва |
|
E класс |
Этиология заболевания |
|
Ec |
Врожденное заболевание |
|
Ep |
Первичное заболевание |
|
Esi |
Вторичное заболевание (интравенозное повреждение) |
|
Ese |
Вторичное заболевание (экстравенозное повреждение) |
|
En |
Не удается установить этиологический фактор |
|
A класс |
Анатомия |
|
As |
Поверхностные вены |
|
Ap |
Перфорантные вены |
|
Ad |
Глубокие вены |
|
An |
Не удается выявить изменения в венозной системе |
|
P класс |
Патогенез |
|
Pr |
Рефлюкс |
|
Po |
Обструкция |
|
Pro |
Рефлюкс и обструкция |
|
Pn |
Не удается установить патогенетический фактор |
|
L |
Уровень диагностики |
|
LI |
Клинический осмотр + ультразвуковая допплерография |
|
LII |
Клинический осмотр + дуплексное сканирование вен |
|
LIII |
Клинический осмотр + дуплексное сканирование вен + флебография или мультиспиральная компьютерная томография или магнитно-резонансная томография |
Таблица 2. Названия отделов венозной системы нижних конечностей в соответствии с международной классификацией хронических заболеваний вен нижних конечностей
|
1 |
Поверхностные |
Telangiectasia |
Tel |
Телангиэктазы |
|
1 |
|
Reticular veins |
Ret |
Ретикулярные вены |
|
2 |
|
Great saphenous vein |
GSVa |
БПВ выше колена |
|
3 |
|
Great saphenous vein |
GSVb |
БПВ ниже колена |
|
4 |
|
Small saphenous vein |
SSV |
Малая подкожная вена |
|
|
|
Anterior accessory saphenous vein |
AASV |
Передняя добавочная подкожная вена |
|
5 |
|
|
NSV |
Несафенные вены |
|
6 |
Глубокие |
Inferior vena cava |
IVC |
Нижняя полая вена |
|
7 |
|
Common iliac vein |
CIV |
Общая подвздошная вена |
|
8 |
|
Internal iliac vein |
IIV |
Внутренняя подвздошная вена |
|
9 |
|
External iliac vein |
EIV |
Наружная подвздошная вена |
|
10 |
|
Pelvic veins |
PELV |
Тазовые вены |
|
11 |
|
Common femoral vein |
CFV |
Общая бедренная вена |
|
12 |
|
Deep femoral vein |
DFV |
Глубокая бедренная вена |
|
13 |
|
Femoral vein |
FV |
Бедренная вена |
|
14 |
|
Popliteal vein |
POPV |
Подколенная вена |
|
15 |
|
Crural (tibial) vein |
TIBV |
Межмышечные (берцовые) вены |
|
15 |
|
Peroneal vein |
PRV |
Малоберцовая вена |
|
15 |
|
Anterior tibial vein |
ATV |
Передняя большеберцовая вена |
|
15 |
|
Posterior tibial vein |
PTV |
Задняя большеберцовая вена |
|
16 |
|
Muscular veins |
MUSV |
Мышечные вены |
|
16 |
|
Gastrocnemius vein |
GAV |
Вены икроножной мышцы (суральные) |
|
16 |
|
Soleal vein |
SOV |
Вены камбаловидной мышцы |
|
17 |
Перфоранты |
Thigh perforator vein |
TPV |
Перфоранты бедра |
|
18 |
|
Calf perforator vein |
CPV |
Перфоранты голени |
1.4.2. Флебэктатическая корона
В раздел «С» редакции классификации CEAP 2020 введен пункт Corona phlebectatica (флебэктатическая корона) в качестве клинического подкласса C4c. Введение данного пункта связано с тем, что флебэктатическая корона может быть предиктором развития более тяжелого типа трофических расстройств [11]. Это предиктивное значение имеет высокую чувствительность (91%), но пограничную специфичность (52%). Наличие флебэктатической короны является клиническим симптомом хронической венозной недостаточности, что следует дифференцировать от простых ретикулярных вен и телеангиэктазий и требует более углубленной диагностики причин ХВН (см. Рекомендацию 7, раздел 2.2. Физикальное обследование).
1.4.3. "Ретикулярный варикоз"
В англоязычной профессиональной литературе для обозначения ретикулярных вен используется термин reticular veins (ретикулярные вены), в то время как термин varicose veins (варикозные вены) применяется только по отношению к классу С2 CEAP (при наличии варикозного расширения подкожных вен, варикозной болезни).
В русскоязычном информационном пространстве широко распространен термин «ретикулярный варикоз», хотя он практически не используется в русскоязычной научной литературе. Применение такого термина приводит к смешению понятий варикозного расширения подкожных вен (класс С2) и расширения внутрикожных вен (класс С1). Вместе с тем, классы C1 и C2 существенно различаются по клинической и прогностической значимости. Использование термина «ретикулярный варикоз» создает условия для преувеличения клинического значения наличия ретикулярных вен.
Не рекомендуется при описании ретикулярных вен и формулировании диагноза использовать термин «ретикулярный варикоз». Корректной формулировкой является «Ретикулярные вены и телеангиэктазии нижних конечностей».
1.4.4. Пример формулировки диагноза.
Допустимо обозначение Ep или En в диагнозе РВ и ТАЭ. Допустимо обозначение Pr:Tel,Ret или Pn в диагнозе РВ и ТАЭ.
Пациентка обратилась к флебологу 15.08.2020. Предъявляет жалобы на наличие расширенных вен и сосудистых звездочек на левой нижней конечности, боли и тяжесть в икроножных мышцах во второй половине дня. Выполнено дуплексное сканирование вен нижних конечностей : глубокие и поверхностные вены – без патологии. Примеры формулировки диагноза:
- Ретикулярные вены и телеангиэктазии нижних конечностей C1sEpAsPn LII 15.08.2020. I.87.8
- Ретикулярные вены и телеангиэктазии нижних конечностей,
Dxt: C1S En As Pr:Tel,Ret LII - 15.08.2020
Sin: C1S En As Pr:Tel,Ret LII - 15.08.2020
1.5. Клиническая картина заболевания и состояния (группы заболеваний или состояний)
Ретикулярные вены и телеангиэктазии нижних конечностей представляют из себя расширение вен от 0.1 до 3 мм в диаметре, локализующиеся чаще всего на наружной поверхности бедер, задней и внутренней поверхностях голени. В большинстве своём они имеют древовидную структуру, цвет - от розового до фиолетового оттенка.
2. Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
2.0. Критерии установления диагноза (состояния)
Критерием для установления диагноза ретикулярые вены и телеангиэктазии нижних конечностей является наличие расширенных и извитых подкожных вен 1-3 мм в диаметре и/или расширенных внутрикожных вен менее 1 мм в диаметре.
2.1. Жалобы и анамнез
- Рекомендация 1. При обследовании пациента с РВ и ТАЭ рекомендовано акцентировать внимание на поиске веноспецифических жалоб и симптомов.
УДД 5 УУР C [2, 9, 10]
Комментарий. В большинстве своем основной жалобой пациентов с другими уточненными поражениями вен является эстетический дискомфорт. В редких случаях наличие ретикулярных вен и телеангиэктазий может сочетаться с веноспецифическими жалобами, такими как отек и венозная боль. При сочетании ретикулярных вен и телеангиэктазий с варикозным расширением вен нижних конечностей, следует акцентировать внимание на жалобах, характерных для этого состояния.
- Рекомендация 2. При опросе пациента с РВ и ТАЭ рекомендовано выяснить наличие аллергии на известные склерозанты, уточнить ведется ли прием оральных контрацептивов или препаратов для менопаузальной гормональной терапии (МГТ), препаратов железа, #миноциклина.
УДД 4 УУР В [12-18]
Комментарий 1. При сборе анамнеза следует уточнить наличие пищевой или лекарственной аллергии, препаратов железа, миноциклина и склонности к кровотечениям, так как данные факторы могут влиять на возможность возникновения осложнений после склеротерапии, а именно вторичных телеангиэктазий и гиперпигментации кожи.
Комментарий 2. При сборе анамнеза следует уточнить, ведется ли прием гормональных контрацептивов или препаратов для МГТ. Сам по себе прием указанных препаратов не всегда является противопоказанием к проведению склеротерапии, однако, как указано в инструкции к препарату на основе полидоканола, противопоказанием к склеротерапии является повышенный риск венозных тромбоэмболических осложнений у пациентов с несколькими факторами риска, включая прием гормональных препаратов, ожирение, курение. При принятии решения о проведении склеротерапии на фоне приема пациенткой контрацептивов или препаратов для МГТ рекомендуется свериться с актуальной инструкцией к склерозанту на сайте Государственного реестра лекарственных средств.
- Рекомендация 3. У пациентов с РВ и ТАЭ при планировании склеротерапии рекомендовано уточнить наличие в анамнезе тромбоза глубоких вен и документированной тромбофилии.
УДД 5 УУР С [2, 9, 10, 19]
Комментарий. Наличие в анамнезе у пациента с РВ и ТАЭ перенесенного венозного тромбоза и документированной наследственной тромбофилии увеличивает риск развития тромбоэмболических осложнений во время проведения склеротерапии, в связи с этим предлагается выявлять такую группу пациентов для рассмотрения возможности проведения медикаментозной тромбопрофилактики после склеротерапии. [19].
- Рекомендация 4. При сборе анамнеза у пациентов с РВ и ТАЭ рекомендовано выяснить проводилось ли раннее устранение ретикулярных вен и телеангиэктазий и каким методом.
УДД 5 УУР С [9]
Комментарий. Важно знать, проводилось ли раньше лечение по поводу устранения ретикулярных вен и телеангиэктазии, какой использовался метод и оценить его эффективность.
- Рекомендация 5. При сборе анамнеза у пациента с РВ и ТАЭ рекомендовано выяснить планируется ли в ближайшие 1-2 года беременность
УДД 4 УУР С [9, 20]
Комментарий. Следует уточнить планирует ли пациентка в ближайшее время (1-2 года) беременность, так как этот фактор может снизить эффективность проведенного лечения [20].
2.2. Физикальное обследование
- Рекомендация 6. Мы рекомендуем осматривать пациентов с РВ и ТАЭ в теплом помещении и при дневном свете.
УДД 5 УУР С [2, 9]
Комментарий. Холод приводит к спазму мелких внутрикожных сосудов, а яркое освещение придает отблеск коже, все это значительно снижает диагностическую эффективность клинического осмотра.
- Рекомендация 7. При клиническом осмотре пациентов с РВ и ТАЭ мы рекомендуем проводить дифференцированную диагностику между простыми телеангиэктазиями и наличием флебэктатической короны.
УДД 4 УУР В [21, 22]
Комментарий. Наличие флебэктатической короны является клиническим симптомом хронической венозной недостаточности, что следует дифференцировать от простых ретикулярных вен и телеангиэктазий и требует более углубленной диагностики причин ХВН [21, 22].
2.3. Лабораторные диагностические исследования
- Рекомендация 8. Лабораторное обследование пациентов с РВ и ТАЭ не рекомендовано
УДД 5 УУР C [2, 9, 10]
2.4. Инструментальные диагностические исследования
- Рекомендация 9. Рутинное ультразвуковое сканирование вен нижних конечностей пациентам с РВ и ТАЭ не рекомендовано.
УДД 2 УУР A [2, 10]
- Рекомендация 10. Всем пациентам с РВ и ТАЭ планирующим склеротерапию или чрескожную лазерную коагуляцию, а также тем, кто имеет рецидивные телеангиэктазии и ретикулярные вены, рекомендовано проведение ультразвукового сканирования вен нижних конечностей.
УДД 2 УУР A [10, 23]
Комментарий. Обязательное ультразвуковое сканирование вен нижних конечностей пациентам с ретикулярными венами и телеангиэктазиями для подтверждения диагноза не рекомендовано, диагноз ставится клинически. Перед проведением лечения (склеротерапия и/или чрескожная лазерная коагуляция), а также пациентам с рецидивом телеангиэктазий и ретикулярных вен проведение ультразвукового сканирования вен нижних конечностей позволяет уточнить клапанную состоятельность глубоких и поверхностных вен, повреждение которой меняет тактику лечения пациента [23].
2.5. Иные диагностические исследования
Пациентам с РВ и ТАЭ не требуется выполнение иных диагностических исследований
2.6. Критерии установления заболевания или состояния (группы заболеваний или состояний)
Диагноз «ретикулярные вены и телеангиэктазии» устанавливается на основании: клинической картины заболевания и данных ультразвукового сканирования вен нижних конечностей, в соответствии с международной классификацией хронических заболеваний вен нижних конечностей (CEAP)
3. Лечение, включая медикаментозную и немедикаментозную терапию, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.0. Общие положения и тактика лечения
Целью лечения при наличии ретикулярных вен и телеангиэктазий является их устранение или уменьшение количества для уменьшения косметического дефекта, ослабления или устранения локальных симптомов и профилактики осложнений, ассоциированных с наличием РВ и ТАЭ (кровотечение из ретикулярных вен и телеангиэктазий).
- Рекомендация 12. Рекомендуется использовать склеротерапию, чрескожную лазерную коагуляцию (ЧЛК) или сочетание склеротерапии и ЧЛК у пациентов с С1 классом ХЗВ для устранения ТАЭ
УДД 1 УУР А [24-29]
- Рекомендация 13. Рекомендуется использовать склеротерапию, чрескожную лазерную коагуляцию (ЧЛК) или сочетание склеротерапии и ЧЛК у пациентов с С1 классом ХЗВ для устранения РВ
УДД 2 УУР В [30-33]
- Рекомендация 14. При наличии РВ и ТАЭ, а также патологического рефлюкса по магистральным подкожным венам, рекомендуется обсудить с пациентом целесообразность предварительного устранения рефлюкса методом химической или термической облитерации
УДД 5 УУР В [9, 10]
- Рекомендация 15. Пациентам с РВ и ТАЭ, планирующим беременность в ближайшие 1-2 года, не рекомендовано устранение РВ и ТАЭ
УДД 5 УУР C [9, 20]
Комментарий. Основными целями лечения ретикулярных вен и телеангиэктазий являются: 1) устранение эстетического дефекта, 2) устранение локальных симптомов в зоне ретикулярных вен и крупных телеангиэктазий, 3) предупреждение кровотечения из ретикулярных вен и телеангиэктазий. Для достижения названных целей могут быть использованы склеротерапия, чрескожная лазерная коагуляция и сочетание этих методов лечения. В настоящее время нет достоверных данных в пользу того или иного метода, той или иной техники проведения данных процедур, результаты лечения с применением обоих методов сопоставимы [25-28]. По данным некоторых исследований ЧЛК имеет преимущества для устранения телеангиэктазий, диаметр которых меньше 1 мм [26, 29]. В некоторых исследованиях был отмечен лучший результат после комбинированного лечения, но качество самих исследований было невысоким [30-33]. Тактика лечения и выбор метода определяются в первую очередь уровнем профессиональной подготовки специалиста и оснащением клиники. Однако существует ряд ограничений для склеротерапии: боязнь иглы, аллергическая реакция на склерозант, телеангиэктазии крайне малого диаметра или вторичные телеангиэктазии [28,34], которые смещают предпочтения в выборе метода в сторону ЧЛК.
3.1. Склеротерапия
- Рекомендация 16. Склеротерапия рекомендована пациентам с С1 классом ХЗВ для устранения ретикулярных вен и ТАЭ
УДД 1 УУР A [24]
Комментарий. Склеротерапия — метод устранения ретикулярных вен и телеангиэктазий с использованием химических веществ, задачей которого является полное разрушение эндотелия и субэндотелиальных структур и частичное разрушение коллагена, что приводит к прекращению функционирования и исчезновению вен [35]. Склеротерапия является наиболее эффективным, легко воспроизводимым, недорогим и относительно безопасным методом [36-41].
3.1.1. Показания и противопоказания к склеротерапии
- Рекомендация 17. Мы рекомендуем учитывать следующие показания к склеротерапии у пациентов с РВ и ТАЭ: устранение эстетического дефекта, устранение локальных симптомов в зоне ретикулярных вен и крупных (0,8–2 мм) телеангиэктазий, предупреждение кровотечения из ретикулярных вен и телеангиэктазий
УДД 5 УУР B [9]
- Рекомендация 18. Мы рекомендуем учитывать следующие абсолютные и относительные противопоказания к склеротерапии у пациентов с РВ и ТАЭ. Абсолютные противопоказания: известная аллергия на склерозант, острый ТГВ и/или ТЭЛА, локальный инфекционный процесс в зоне предполагаемой инъекции или генерализованная инфекция, длительный постельный режим или иммобилизация, наличие известного инструментально подтвержденного сброса крови справа налево (открытое овальное окно) при использовании пенной формы. Относительные противопоказания: беременность, период лактации (если решено выполнить склеротерапию, рекомендуется прекратить грудное вскармливание на 2—3 дня), тяжелые формы облитерирующих заболеваний артерий нижних конечностей (хроническая артериальная недостаточность IIб - IV степени), наличие декомпенсированной хронической патологии, высокий риск ВТЭО (острый тромбоз подкожных вен, эпизоды ВТЭО в анамнезе, известная наследственная тромбофилия, подтвержденное состояние гиперкоагуляции, активный рак и др.), неврологические нарушения, включая мигрень, наблюдавшиеся при ранее выполненных сеансах склеротерапии
УДД 5 УУР В [10, 42-45]
- Рекомендация 19. Мы рекомендуем не считать противопоказанием к склеротерапии ретикулярных вен и телеангиэктазий прием антикоагулянтов у пациентов с С1 классом ХЗВ
УДД 1 УУР А [46-48]
Комментарий. Необходимо учитывать противопоказания, перечисленные в официальной инструкции к препарату для склеротерапии. Несмотря на то, что в инструкциях к препаратам для склеротерапии курение относится к одному из факторов риска развития ВТЭО, результаты исследований, оценивающих взаимосвязь курения и ВТЭО, неоднозначны [49-51].
3.1.2. Методы склеротерапии
- Рекомендация 20. Для склеротерапии у пациентов с С1 классом ХЗВ рекомендуется использовать препараты из клинико-фармакологической группы препаратов для склерозирования варикозно расширенных вен (полидоканол (C05BB02), натрия тетрадецил сульфат (C05BB04)) в виде раствора или пены
УДД 1 УУР А [24]
Комментарий. По механизму действия полидоканол (C05BB02), натрия тетрадецил сульфат (C05BB04) относятся к детергентам.
- Рекомендация 21. При проведении склеротерапии РВ у пациентов с С1 классом ХЗВ рекомендуется использовать концентрацию не выше 1% для полидоканола и 0,5% для натрия тетрадецил сульфата
УДД 1 УУР А [24, 38, 52, 53]
- Рекомендация 22. При проведении склеротерапии ТАЭ у пациентов с С1 классом ХЗВ рекомендовано использовать концентрацию полидоканола не выше 0,5% и натрия тетрадецил сульфата не выше 0,2%
УДД 1 УУР A [24 38, 52, 53]
- Рекомендация 23. При проведении склеротерапии РВ у пациентов с С1 классом ХЗВ рекомендовано использовать #глюкозу (V06DC01) 75%
УДД 2 УУР С [54]
- Рекомендация 24. При проведении склеротерапии ТАЭ у пациентов с С1 классом ХЗВ рекомендовано использовать #глюкозу (V06DC01) 75%
УДД 4 УУР С [55, 56]
Комментарий. В Российской Федерации для проведения склеротерапии разрешены к применению натрия тетрадецил сульфат и полидоканол (код ATX: C05BB02 (Polidocanol), действующее вещество - лауромакрогол-400). Оба препарата как в виде раствора, так и в виде пены в эквивалентных концентрациях вызывают одинаковые гистологические изменения, обладают сходной эффективностью и переносимостью. Не было отмечено различий между двумя препаратами в эффективности и частоте побочных явлений [52, 53]. Следует помнить, что при увеличении концентрации склерозанта увеличивается риск побочных реакций [38] Частота побочных явлений увеличивается при применении пенной формы склерозанта для склеротерапии ТАЭ [57].
Результаты исследований, сравнивающих склеротерапию ретикулярных вен и ТАЭ с использованием пенной и жидкой форм, неоднозначны. В некоторых работах выявлена одинаковая их эффективность [39], однако имеются данные о преимуществе пенной формы, но ее применение сопровождается большей частотой побочных реакций [58].
Имеются исследования, доказавшие эффективность и безопасность применения в качестве склерозанта 75% раствора глюкозы [54-56].
- Рекомендация 25. При склеротерапии ретикулярных вен и ТАЭ у пациентов с С1 классом ХЗВ рекомендуется использовать жидкую форму склерозанта
УДД 2 УУР В [38, 52, 53]
Комментарий. Эффективность жидкой формы склерозанта доказана при любом диаметре вен [38, 52, 53]. При наличии явно определяемых визуально ретикулярных вен и ТАЭ введение склерозанта допустимо без использования устройств для визуализации (веновизоров). Их применение в первую очередь может помочь в визуализации питающих ТАЭ ретикулярных вен и тем самым улучшить результаты склеротерапии.
- Рекомендация 26. Пенную форму склерозанта рекомендуется использовать для склеротерапии ретикулярных вен у пациентов с С1 классом ХЗВ
УДД 2 УУР В [59]
- Рекомендация 27. Для склеротерапии РВ у пациентов с С1 классом ХЗВ пенную форму склерозанта рекомендуется готовить по методике L. Tessari
УДД 2 УУР B [59-61]
Комментарий. Для приготовления пенной формы склерозанта допустимо использование нестерильного атмосферного воздуха. Это не несет угрозы бактериальной контаминации, что позволяет не прибегать к использованию стерильных воздушных смесей [62, 63]. Общепринято приготовление пены по L. Tessari (с помощью двух шприцев, соединенных через трехходовый переходник) путем смешивания склерозанта и атмосферного воздуха в соотношении 1:2 или 1:4 [59-61]. Для внутривенного введения пены некоторые исследователи рекомендуют использовать иглу диаметром не менее 25G. При использовании иглы диаметром менее 25G микропузырьки пены разрушаются при прохождении через просвет, что снижает активность склерозирующего агента [64]. Однако исследований, в которых сравнивался бы результат склеротерапии в зависимости от диаметра иглы, нет. Поэтому вопрос о выборе иглы для микросклеротерпии остается дискутабельным. Исследования показали, что введение больших объемов пены (более 10 мл), приготовленной на основе смеси углекислого газа и кислорода, ассоциируется с меньшим числом неврологических расстройств [65, 66], при использовании меньших объемов пены (до 10 мл) уменьшения частоты подобных осложнений не наблюдалось [67, 68]. До 30% общей популяции имеют открытое овальное окно, которое обеспечивает возможность проникновения пузырьков воздуха в систему церебральных артерий. Эта цифра существенно превышает частоту возникновения неврологических нарушений при выполнении пенной склеротерапии. Более того, на сегодняшний день убедительно доказана лишь взаимосвязь открытого овального окна и ишемического инсульта, но не прочих неврологических реакций [69, 70]. Таким образом, тотальный скрининг всех пациентов на предмет сброса крови справа налево перед проведением склеротерапии считается нецелесообразным.
3.1.3. Компрессия после склеротерапии
- Рекомендация 28. Рекомендуется рассмотреть целесообразность проведения компрессионной терапии (медицинский компрессионный трикотаж или компрессионный бандаж) после склеротерапии РВ и ТАЭ у пациентов с С1 классом ХЗВ с учетом особенностей клинического случая и предпочтений пациента
УДД 2 УУР В [39, 71-73]
Комментарий. В некоторых исследованиях была выявлена польза компрессии в течение 3 недель после склеротерапии ретикулярных вен и ТАЭ, проявляющаяся в сокращении площади поражения, уменьшении пигментации и гематом [72, 73], однако, по данным других исследований [41], компрессия не влияла на частоту пигментаций и вторичных ТАЭ. Необходимы дальнейшие рандомизированные контролируемые исследования для установления роли компрессии после склеротерапии. На сегодняшний день показания к применению компрессии и ее режим не могут быть регламентированы.
3.1.4. Период после склеротерапии
- Рекомендация 29. Для оценки результатов склеротерапии РВ и ТАЭ у пациентов с С1 классом ХЗВ рекомендуется проводить клинический осмотр пациента.
УДД 5 УУР С [9]
Комментарий. Количество сеансов склеротерапии и временные интервалы между сеансами не могут быть регламентированы из-за субъективизма оценки промежуточного результата. Конечный результат принято считать хорошим, если визуально отсутствуют измененные сосуды или достигнуто существенное уменьшение их количества, нет выраженных нарушений пигментации, вторичных телеангиэктазий.
3.1.5. Побочные реакции и осложнения склеротерапии
- Рекомендация 30. У пациентов с С1 классом ХЗВ рекомендовано считать осложнением склеротерапии следующие состояния: анафилактический шок, поверхностные некрозы кожи, Embolia cutis medicamentosa, неврологические симптомы, тромбофлебит подкожных вен, тромбоз глубоких вен, тромбоэмболия легочной артерии
УДД 4 УУР С [74-82, 84-89]
- Рекомендация 31. У пациентов с С1 классом ХЗВ рекомендовано считать побочной реакцией склеротерапии следующие состояния: гиперпигментация, вторичные телеангиэктазии
УДД 2 УУР А [77, 83]
Комментарий. Анафилактический шок, требующий интенсивной терапии, при склеротерапии развивается казуистически редко, кожные реакции в виде крапивницы также представляют собой нечастое явление [74, 75].
Поверхностные некрозы кожи возникают редко и развиваются либо при паравазальном введении высококонцентрированного склерозанта за счет специфического повреждения тканей, либо при быстром введении под избыточным давлением больших объемов склерозанта любой концентрации (в том числе низкой) за счет его проникновения в артериальное микроциркуляторное русло или рефлекторного ангиоспазма [76-79]. В существующей на настоящее время литературе [80] указывается, что во время склеротерапии ретикулярных вен и ТАЭ при паравазальном введении полидоканола кожные некрозы могут возникать при введении пенной формы 0,5 мл 2% полидоканола или жидкой формы 0,5 мл 1% полидоканола. При введении паравазально менее 0,5 мл полидоканола в любой концентрации кожные некрозы не развивались.
Embolia cutis medicamentosa (синдром Николау) — формирование обширных некрозов в зоне лечения происходит чрезвычайно редко [81, 82].
Гиперпигментация кожи наблюдается в 0,3—78% случаев и чаще всего спонтанно медленно регрессирует, исчезая у 70—90% пациентов в течение 1-го года после склеротерапии [77, 83]. Большая частота пигментаций наблюдается при введении склерозантов в высоких концентрациях [57]. По данным некоторых исследований [73], пигментация менее выражена при использовании компрессии после склеротерапии в течение 3 нед. Несколько чаще она возникает при пенной склеротерапии [84].
Вторичные ТАЭ — индивидуальная и непредсказуемая реакция в виде появления большого количества очень малого калибра ТАЭ в зоне склеротерапии. Частота этого нежелательного явления составляет 5—21%. Причиной возникновения вторичных ТАЭ может быть неадекватная обработка всех источников рефлюкса, введение склерозантов в высокой концентрации или большом объеме [77].
Неврологические симптомы в виде преходящих нарушений зрения, головных болей, мигрени, парестезий и дисфазии встречаются чрезвычайно редко, могут быть связаны с проведением склеротерапии любым способом, но более характерны для введения пенной формы препарата [84-87].
Тромбофлебит склерозированных вен не имеет убедительного разграничения с нормальной воспалительной реакцией, сопровождающей облитерацию подвергшейся вмешательству вены. Истинным тромбофлебитом следует считать появление воспалительной реакции в вене, которая не подвергалась склеротерапии [76, 84].
ТГВ и ТЭЛА являются исключительно редкими осложнениями склеротерапии. Использование больших объемов склерозанта, в частности пенной формы, ассоциируется с повышенной частотой ТГВ [88, 89].
3.1.6. Профилактика и лечение осложнений и побочных реакций склеротерапии
- Рекомендация 32. При появлении аллергической реакции следует остановить процедуру и действовать согласно алгоритму действий при аллергических реакциях
УДД 5 УУР B [76]
- Рекомендация 33. При возникновении сильной боли во время введения склерозанта рекомендовано немедленно прекратить процедуру. При подозрении на попадание склерозанта в артериальное русло необходимо ввести лечебную дозу нефракционированного гепарина (5000 МЕ) или низкомолекулярного гепарина (из расчета мг/кг массы тела согласно инструкции) системно
УДД 5 УУР В [76]
- Рекомендация 34. Во избежание возникновения кожных некрозов не рекомендуется вводить склерозант под избыточным давлением, рекомендуется использовать низкие концентрации склерозанта
УДД 2 УУР В [76-82]
- Рекомендация 35. Способами уменьшения риска возникновения стойкой гиперпигментации рекомендуется считать:
- использование склерозанта в рекомендованных для РВ и ТАЭ концентрациях;
- применение эластической компрессии;
- удаление сгустков крови из просвета облитерированной вены через 2—3 недели после склеротерапии.
УДД 3 УУР В [73, 90]
- Рекомендация 36. С целью снижения риска вторичных ТАЭ при проведении склеротерапии рекомендуется устранять все возможные источники рефлюкса, не применять склерозант в высоких концентрациях и большом объеме, не вводить его под избыточным давлением, применять компрессионный трикотаж после процедуры
УДД 3 УУР В [72, 77]
- Рекомендация 37. При возникновении вторичных ТАЭ рекомендуется выжидательная тактика в течение нескольких месяцев. Для устранения фиолетовых вторичных ТАЭ целесообразно выполнить ДСВНК или визуализацию с помощью веновизора с целью выявления питающей вены и ее последующей склеротерапией. Для устранения красных вторичных ТАЭ рекомендуется использовать транскутанный лазер или склеротерапию низко концентрированными растворами склерозантов, а также осмотические склерозанты
УДД 3 УУР В [59,72, 91]
- Рекомендация 38. Пациентам, страдающим мигренью, а также при наличии анамнестических указаний на возникновение неврологических реакций при ранее выполненной склеротерапии рекомендуется проводить процедуру лишь в том случае, если индивидуальная польза значительно превышает риск, отдавать предпочтение жидкой форме склерозанта, избегать введения больших объемов препарата [84, 85, 86, 87]. Возможно использование осмотических склерозантов
УДД 3 УУР В [54-56]
Комментарий. Так как это осложнение встречается крайне редко, и в литературе описаны единичные случаи, невозможно указать точный объем препарата, который с большой долей вероятности вызвал бы его возникновение.
- Рекомендация 39. Пациентам с высоким индивидуальным риском ВТЭО (наличие эпизодов ВТЭО в анамнезе, верифицированная наследственная тромбофилия) рекомендуется проводить фармакопрофилактику в соответствии с актуальными рекомендациями по профилактике и лечению венозных тромбоэмболических осложнений, использовать эластичную компрессию, избегать введения больших объемов склерозанта, проводить максимально раннюю активизацию после выполнения инъекции
УДД 3 УУР В [91]
3.2. Чрескожная лазерная коагуляция
3.2.1. Показания к чрескожной лазерной коагуляции
- Рекомендация 40. Чрескожная лазерная коагуляция может быть рекомендована, как альтернатива склеротерапии, в следующих ситуациях: у пациентов с фобией к инъекциям, при непереносимости склерозантов, при телеангиэктазиях, устойчивых к склеротерапии, при вторичных телеангиэктазиях (matting), при выраженной гиперпигментации на склеротерапию в анамнезе, при крайне маленьком диаметре ТАЭ, высоком риске ВТЭО
УДД 2 УУР В [2, 92-96]
Комментарий. В отличие от склерозантов, для лазеров нет ограничений по максимальной общей дозе излучения на одну процедуру, нет рисков анафилактического шока. Лазерное лечение можно проводить без использования компрессионного трикотажа [2, 96].
3.2.2. Противопоказания к чрескожной лазерной коагуляции
- Рекомендация 41. Мы рекомендуем считать противопоказанием к чрескожной лазерной коагуляции при лечении пациентов с ретикулярными венами и телеангиэктазиями следующие состояния: фотодерматозы, порфирия, фотосенсебилизация, загар (3-4 недели до начала лечения), солнечные ожоги, активная вирусная или бактериальная инфекция, острый венозный тромбоз, беременность, активный онкологический процесс, эпилепсия, гипопигментация (витилиго), келоидные рубцы, холодовая аллергия, хроническая артериальная недостаточность, хронические кожные заболевания в стадии обострения.
УДД 5 УУР В [2, 98-102]
3.2.3. Подготовка к чрескожной лазерной коагуляции
- Рекомендация 42. Перед проведением чрескожной лазерной коагуляции рекомендуется информировать пациента об альтернативных методах лечения, методике выполнения, ожидаемых результатах, возможных побочных реакциях, осложнениях и мерах по их предупреждению
УДД 5 УУР А [97, 98, 102]
Комментарий. Некоторые специалисты рекомендуют пациентам избегать воздействия солнца (искусственного загара) или использовать солнцезащитные средства (SPF 50) в течение 3-4 недель до и после лазерного лечения, однако убедительных данных о пользе такой рекомендации на сегодняшний день нет. Лазерная обработка кожи, покрытой лосьонами или мазями, может привести к ожогам кожи и гиперпигментации. Следовательно, следует обязательно удалить все лишнее с кожи перед лазерным лечением. Чрескожная лазерная коагуляция у пациентов с загорелой кожей должна проводиться с осторожностью, на более низких энергетических параметрах. Для выявления пациентов, предрасположенных к реакциям идиопатической гиперчувствительности, рекомендована пробная обработка небольшого участка кожи перед проведением полного сеанса лечения, особенно у пациентов с темными фототипами кожи (IV-VI по Фитцпатрику, см. Приложение Г1. Классификация фотопипа кожи Фитцпатрика) [2, 95, 98, 103].
3.2.4. Выбор длины волны лазерного аппарата
- Рекомендация 43. При поверхностных ТАЭ диаметром менее 1 мм и вторичных телеангиэктазиях (matting) рекомендовано применение лазеров PDL (585 - 600 нм) и KTP (532 нм)
УДД 3 УУР В [104-108]
- Рекомендация 44. У пациентов с телеангиэктазиями и ретикулярными венами диаметром до 3 мм мы рекомендуем применять длинноимпульсные лазеры Nd: YAG (1064 нм)
УДД 2 УУР В [109-112]
- Рекомендация 45. При неэффективности PDL (585 - 600 нм), KTP (532 нм) или Nd: YAG (1064 нм) лазеров у пациентов с внутрикожными венами диаметром 1-3 мм возможно применение александритового лазера (755 нм) и диодных лазеров (800-983 нм)
УДД 4 УУР С [113-116]
Комментарий. Выбор длины волны определяет, в основном, может ли световая энергия проходить через наружные слои кожи и, таким образом, достигать цели, в данном случае венозного сосуда. Между длинами волн 600 нм -1200 нм кожа человека имеет так называемое оптическое окно, с минимальным поглощением энергии. Хромофоры кожи человека, которые отвечают за поглощение электромагнитной энергии в этой части спектра — это гемоглобин в дерме и меланин в эпидермисе. Вода начинает иметь значение только в инфракрасной части этого спектра на длинах волн выше 1000 нм. При этом длина волны 532 нм примерно в 100 раз сильнее поглощается гемоглобином, чем 1064 нм. То же самое верно и для меланина, который поглощает волны длиною 532 нм примерно в восемь раз сильнее, чем волны длиною 1064 нм. Поглощение водой не играет особой роли на обеих длинах волн. Таким образом, лазер с длиною волны 532 нм проникает в кожу существенно менее глубоко, чем с длиной 1064 нм. При использовании длины волны, которая слишком сильно поглощается гемоглобином в сосудах большого диаметра, нижняя стенка сосуда не нагревается в достаточной степени, поскольку энергия преимущественно поглощается в той части, на которую сначала попадает лазерный луч. Напротив, длина волны, более умеренно поглощаемая гемоглобином, способна нагревать весь сосуд. По этой причине более крупные сосуды диаметром порядка 1 мм не могут быть успешно обработаны лазером с короткими длинами волн, такими как 532 нм, 585 нм или даже 595 нм [117-119].
3.2.5. Параметры чрескожной лазерной коагуляции
3.2.5.1. Общие принципы подбора параметров чрескожной лазерной коагуляции
- Для достижения максимального эффекта чрескожной лазерной коагуляции необходимо правильное сочетание длины волны, флюэнса, длительности импульса и диаметра пятна лазера [2, 92, 97, 103, 117].
- Чем глубже расположен сосуд, тем больше размер пятна, больше длина волны, больше продолжительность импульса
- Чем меньше диаметр сосуда, тем меньше размер пятна и короче продолжительность импульса, а плотность потока энергии выше
- Чем больше диаметр сосуда, тем больше размер пятна и продолжительность импульса, а плотность потока энергии меньше
- Чем темнее фототип кожи, тем больше длина волны, продолжительнее импульс и интервал между импульсами, важно эффективное охлаждение
- Для достижения эффекта обычно необходимо несколько процедур, также повысить эффективность может несколько проходов во время процедуры.
- Интервал между процедурами от 2 до 6 недель, чем темнее кожа, тем больше интервал.
3.2.5.2. Плотность потока лазерной энергии
Плотность потока лазерной энергии - количество излучаемой энергии на единицу площади (флюэнс, J/cm2). Количество лазерной энергии, которая, наконец, достигает целевого сосуда, определяет, будет ли сосуд закрыт. При лечении поверхностных вен достаточный флюэнс вызовет немедленную видимую реакцию, такую как спазм, изменение цвета или тромбоз сосуда. Флюэнс варьирует от 4 Дж/см2 для PDL лазеров при лечении поверхностных сосудов 0,1 мм в диаметре и до 580 Дж/см2 на длинноимпульсных неодимовых лазерах (Nd: YAG). Кроме длины волны, при выборе плотности потока энергии должны учитываться глубина, диаметр и цвета сосуда. Так, например, синие вены содержат больше хромофора и для их обработки необходимы меньшие энергетические параметры по сравнению с тонкими красными сосудами [108, 119, 120].
3.2.5.3. Продолжительность импульса лазера
При подаче желаемого количества лазерной энергии важное значение имеет и время ее доставки. Согласно принципу селективного фототермолиза длительность лазерного импульса должна быть меньше времени тепловой релаксации целевой ткани. Тепловая релаксация описывает временной ход передачи тепла, обычно методом теплопроводности от нагретой целевой структуры к более холодной окружающей ткани. На практике это означает, что если время действия лазерных импульсов превышает время тепловой релаксации целевой ткани, то теряется преимущество более высокого поглощения в целевой ткани. Величину времени тепловой релаксации можно оценить следующим образом: ее значение в секундах составляет примерно квадрат целевого диаметра (например, время тепловой релаксации составляет примерно 250 мс в сосуде диаметром 0,5 мм или примерно 40 мс в сосуде диаметром 0,2 мм). На самом деле время тепловой релаксации немного меньше, чем в приведенных выше примерах, но в любом случае фактическая длительность импульсов должна быть ниже. В то же время действие импульсов не должно быть и слишком коротким. Например, для лазера ND: YAG с длиной волны 1064 нм было показано, что более длительные импульсы от 20 мс до 60 мс стабильно дают лучшие клинические результаты, чем 3 мс длительность импульса в сосудах со средним диаметром 0,8 мм. Гистология подтверждает эти данные, показывая заметное сокращение коллагена при использовании более длинных импульсов, в то время как короткие импульсы продолжительностью 3 мс были способны вызывать только тромботическую окклюзию сосуда. В заключение, можно сказать, что существенное тепловое повреждение вокруг целевой вены или, по крайней мере, значительное тепловое повреждение всей стенки сосуда является необходимым условием для достижения мгновенной и прочной окклюзии вены. С другой стороны, более длительные лазерные импульсы более болезненны, чем короткие, в частности, многие пациенты не переносят импульсы длительностью более 100 мс, что делает иногда их назначение невозможным [118, 121-123].
3.2.5.4. Диаметр пятна лазера
Для успешной лазерной абляции телеангиэктазий нижних конечностей необходимо учитывать фактическую глубину проникновения лазерного света. Интересно, что эта глубина зависит не только от длины волны лазера и его характеристик поглощения, но и от его характеристик рассеивания. Таким образом, фактическая глубина проникновения может быть увеличена путем увеличения диаметра пятна. Из-за упомянутых эффектов рассеивания луч, будучи изначально цилиндрической формы, в тканях становится конусовидным, прежде чем полностью поглощается. Из-за явления прямого рассеивания, лучу требуется больше времени для полного исчезновения, которое происходит на большей глубине ткани при большем диаметре луча [2, 92, 97, 103, 117].
3.2.5.5. Охлаждение кожи
- Рекомендация 46. Мы рекомендуем охлаждение кожи во время процедуры ЧЛК для уменьшения болезненности и профилактики осложнений при работе на любом типе лазеров
УДД 3 УУР В [92, 124-127]
Комментарий. Во избежание термического повреждения кожи важно правильно ее охладить. Подходящими охлаждающими устройствами являются динамическое спрей-охлаждение, контактное охлаждение насадкой или охлажденный воздух. Охлажденные гели и кубики льда не обеспечивают достаточного и однородного охлаждения кожи. Необходимо избегать избыточного давления на кожу и очень низких температур[92, 124-127]
3.2.6. Побочные эффекты и осложнения
- Рекомендация 47. К побочным эффектам и осложнениям чрескожной лазерной коагуляции ретикулярных вен и телеангиэктазий рекомендуется относить: временную или постоянную гиперпигментацию, вторичные телеангиэктазии, гипопигментации, экхимозы, отек и ожоги кожи, рубцевание кожи, реактивация герпетической инфекции, боль во время процедуры, низкая эффективность лечения
УДД 3 УУР В [2, 98, 102, 128-133].
Комментарий. Гиперпигментация, как и гипопигментация, может произойти при использовании любого лазера, но с большей вероятностью она возникает после лечения лазерами с более короткими длинами волн, например, KTP (532 нм). Желательно избегать применения таких лазеров у пациентов с IV-VI фототипами кожи по Фитцпатрику (Приложение Г1. Классификация фотопипа кожи Фитцпатрика) [2, 92, 98, 102].
После лазерного лечения некоторые авторы рекомендуют избегать пребывания на солнце (солярий), применять солнцезащитные средства (SPF 50), пока видна какая-либо кожная реакция, обычно в течение 3–4 недель [97].
Выраженные болевые ощущения во время процедуры могут сигнализировать о высокой вероятности развития осложнений, необходимо снизить энергетические параметры лазера (флюэнс, длительность импульса) и обеспечить эффективное охлаждение. Редкими осложнения лазерного лечения являются ожоги кожи с последующим рубцеванием или без него. Эти побочные эффекты чаще всего возникают при слишком большой дозе лазерной энергии. Это может произойти по следующим причинам [2, 92, 98, 102]:
- Использование слишком высокой плотности энергии
- Случайное суммирование импульсов или непреднамеренное перекрытие импульсов
- Преднамеренное суммирование импульсов, но со слишком малыми интервалами охлаждения между ними
- Неправильное охлаждение поверхности кожи во время лечения
3.2.7. Правила безопасности при работе с лазерами
Аппараты для чрескожной лазерной коагуляции относятся к IV классу опасности, поэтому должны соблюдаться правила безопасности по оборудованию кабинета, защите персонала и пациента в соответствии с действующими санитарно-эпидемиологическими требованиями к организациям, осуществляющим медицинскую деятельность.
3.3. Комбинированное лечение
- Рекомендация 48. Мы рекомендуем использовать длинноимпульсный неодимовый лазер в сочетании со склеротерапией для более эффективного устранения телеангиэктазий и ретикулярных вен в рамках одной лечебной сессии
УДД 2 УРР А [32, 33]
- Рекомендация 49. Мы рекомендуем использовать длинноимпульсный неодимовый лазер через 3 недели после склеротерапии как дополнительный улучшающий результат метод лечения
УДД 3 УРР В [31]
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
После устранения ретикулярных вен и телангиэктазий специфическая реабилитация не требуется.
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
Пациентам с ретикулярными венами и телангиэктазиями нижних конечностей специфическая профилактика и диспансеризация не требуются.
6. Организация оказания медицинской помощи
Медицинская помощь пациентам с ретикулярными венами и телангиэктазиями нижних конечностей оказывается в амбулаторных условиях в виде первичной медико-санитарной помощи врачом-хирургом, врачом сердечно-сосудистым хирургом и врачом-косметологом
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Не предусмотрена
Критерии оказания качества медицинской помощи
|
№ |
Критерии качества |
Выполнена |
|
|
Этап постановки диагноза |
|||
|
1 |
Выполнено клиническое обследование пациента (выявление веноспецифических жалоб, сбор анамнеза, осмотр, пальпации нижних конечностей). |
Да |
Нет |
|
2 |
Определен клинический класс заболевания по CEAP |
Да |
Нет |
|
3 |
Перед проведением инвазивного лечения выполнено дуплексное сканирование вен нижних конечностей с оценкой состояния поверхностных и глубоких вен обеих нижних конечностей |
Да |
Нет |
|
Этап консервативного и хирургического лечения |
|||
|
1 |
При согласии пациента на инвазивное лечение уменьшено количество или устранены ретикулярные вены и телеангиэктазии нижних конечностей, достигнуто ослабление или устранение локальных симптомов |
Да |
Нет |
Список литературы
- Золотухин И., Селиверстов Е., Шевцов Ю., Авакъянц И., Никишков А., Татаринцев А., Кириенко А. Распространенност1. Золотухин И., Селиверстов Е., Шевцов Ю., Авакъянц И., Никишков А., Татаринцев А., Кириенко А. Распространенность хронических заболеваний вен: результаты популяционного эпидемиологического исследования // Флебология. 2016. Т. 10, № 3. С. 119–125.
- Handbook of Venous and Lymphatic Disorders: Guidelines of the American Venous Forum, Fourth Edition. 4-е изд. / под ред. Gloviczki P. и др. Boca Raton: CRC Press, 2017. 866 с.
- Nicolaides A., Kakkos S., Eklof B., Perrin M., Nelzen O., Neglen P., Partsch H., Rybak Z. Management of chronic venous disorders of the lower limbs - guidelines according to scientific evidence // Int Angiol. 2014. Т. 33, № 2. С. 87–208.
- Wittens C., Davies A.H., Bækgaard N., Broholm R., Cavezzi A., Chastanet S., de Wolf M., Eggen C., Giannoukas A., Gohel M., Kakkos S., Lawson J., Noppeney T., Onida S., Pittaluga P., Thomis S., Toonder I., Vuylsteke M., Esvs Guidelines Committee null, Kolh P., de Borst G.J., Chakfé N., Debus S., Hinchliffe R., Koncar I., Lindholt J., de Ceniga M.V., Vermassen F., Verzini F., Document Reviewers null, De Maeseneer M.G., Blomgren L., Hartung O., Kalodiki E., Korten E., Lugli M., Naylor R., Nicolini P., Rosales A. Editor’s Choice - Management of Chronic Venous Disease: Clinical Practice Guidelines of the European Society for Vascular Surgery (ESVS) // Eur J Vasc Endovasc Surg. 2015. Т. 49, № 6. С. 678–737.
- Beebe H.G., Bergan J.J., Bergqvist D., Eklof B., Eriksson I., Goldman M.P., Greenfield L.J., Hobson R.W., Juhan C., Kistner R.L., Labropoulos N., Malouf G.M., Menzoian J.O., Moneta G.L., Myers K.A., Neglen P., Nicolaides A.N., O’Donnell T.F., Partsch H., Perrin M., Porter J.M., Raju S., Rich N.M., Richardson G., Sumner D.S. Classification and grading of chronic venous disease in the lower limbs. A consensus statement // Eur J Vasc Endovasc Surg. 1996. Т. 12, № 4. С. 487–491.
- Eklöf B., Rutherford R.B., Bergan J.J., Carpentier P.H., Gloviczki P., Kistner R.L., Meissner M.H., Moneta G.L., Myers K., Padberg F.T., Perrin M., Ruckley C.V., Smith P.C., Wakefield T.W., American Venous Forum International Ad Hoc Committee for Revision of the CEAP Classification. Revision of the CEAP classification for chronic venous disorders: consensus statement // J Vasc Surg. 2004. Т. 40, № 6. С. 1248–1252.
- Rabe E., Pannier F. Clinical, aetiological, anatomical and pathological classification (CEAP): gold standard and limits // Phlebology. 2012. Т. 27 Suppl 1. С. 114–118.
- Lurie F., Passman M., Meisner M., Dalsing M., Masuda E., Welch H., Bush R.L., Blebea J., Carpentier P.H., De Maeseneer M., Gasparis A., Labropoulos N., Marston W.A., Rafetto J., Santiago F., Shortell C., Uhl J.F., Urbanek T., van Rij A., Eklof B., Gloviczki P., Kistner R., Lawrence P., Moneta G., Padberg F., Perrin M., Wakefield T. The 2020 update of the CEAP classification system and reporting standards // J Vasc Surg Venous Lymphat Disord. J Vasc Surg Venous Lymphat Disord, 2020. Т. 8, № 3. С. 342–352.
- Российские клинические рекомендации по диагностике и лечению хронических заболеваний вен. // Флебология. 2018. Т. 12, № 3. С. 146–240.
- Rabe E., Breu F.X., Cavezzi A., Coleridge Smith P., Frullini A., Gillet J.L., Guex J.J., Hamel-Desnos C., Kern P., Partsch B., Ramelet A.A., Tessari L., Pannier F., Guideline Group. European guidelines for sclerotherapy in chronic venous disorders // Phlebology. 2014. Т. 29, № 6. С. 338–354.
- Carpentier P.H., Cornu-Thénard A., Uhl J.-F., Partsch H., Antignani P.L., Société Française de Médecine Vasculaire, European Working Group on the Clinical Characterization of Venous Disorders. Appraisal of the information content of the C classes of CEAP clinical classification of chronic venous disorders: a multicenter evaluation of 872 patients // J Vasc Surg. 2003. Т. 37, № 4. С. 827–833.
- Nakano L.C., Cacione D.G., Baptista-Silva J.C., Flumignan R.L. Treatment for telangiectasias and reticular veins // Cochrane Database Syst Rev. 2021. Т. 10, № 10. С. CD012723.
- Hamel-Desnos C.M., Gillet J.-L., Desnos P.R., Allaert F.A. Sclerotherapy of varicose veins in patients with documented thrombophilia: a prospective controlled randomized study of 105 cases // Phlebology. 2009. Т. 24, № 4. С. 176–182.
- Uhl J.-F., Cornu-Thénard A., Carpentier P.H., Widmer M.-T., Partsch H., Antignani P.L. Clinical and hemodynamic significance of corona phlebectatica in chronic venous disorders // J Vasc Surg. 2005. Т. 42, № 6. С. 1163–1168.
- Uhl J.-F., Cornu-Thenard A., Satger B., Carpentier P.H. Clinical analysis of the corona phlebectatica // J Vasc Surg. 2012. Т. 55, № 1. С. 150–153.
- Ruckley C.V., Allan P.L., Evans C.J., Lee A.J., Fowkes F.G.R. Telangiectasia and venous reflux in the Edinburgh Vein Study // Phlebology. 2012. Т. 27, № 6. С. 297–302.
- Engelhorn C.A., Engelhorn A.L.V., Cassou M.F., Salles-Cunha S. Patterns of saphenous venous reflux in women presenting with lower extremity telangiectasias // Dermatol Surg. 2007. Т. 33, № 3. С. 282–288.
- Somjen G.M., Ziegenbein R., Johnston A.H., Royle J.P. Anatomical examination of leg telangiectases with duplex scanning // J Dermatol Surg Oncol. 1993. Т. 19, № 10. С. 940–945.
- De Maeseneer M.G., Kakkos S.K., Aherne T., Baekgaard N., Black S., Blomgren L., Giannoukas A., Gohel M., de Graaf R., Hamel-Desnos C., Jawien A., Jaworucka-Kaczorowska A., Lattimer C.R., Mosti G., Noppeney T., van Rijn M.J., Stansby G., Esvs Guidelines Committee null, Kolh P., Bastos Goncalves F., Chakfé N., Coscas R., de Borst G.J., Dias N.V., Hinchliffe R.J., Koncar I.B., Lindholt J.S., Trimarchi S., Tulamo R., Twine C.P., Vermassen F., Wanhainen A., Document Reviewers null, Björck M., Labropoulos N., Lurie F., Mansilha A., Nyamekye I.K., Ramirez Ortega M., Ulloa J.H., Urbanek T., van Rij A.M., Vuylsteke M.E. Editor’s Choice - European Society for Vascular Surgery (ESVS) 2022 Clinical Practice Guidelines on the Management of Chronic Venous Disease of the Lower Limbs // Eur J Vasc Endovasc Surg. 2022. Т. 63, № 2. С. 184–267.
- L S., H M. Sclerotherapy for lower limb telangiectasias // Cochrane Database Syst Rev. Cochrane Database Syst Rev, 2011. Т. 2011, № 12.
- Coles C.M., Werner R.S., Zelickson B.D. Comparative pilot study evaluating the treatment of leg veins with a long pulse ND:YAG laser and sclerotherapy // Lasers Surg Med. 2002. Т. 30, № 2. С. 154–159.
- Ianosi G., Ianosi S., Calbureanu-Popescu M.X., Tutunaru C., Calina D., Neagoe D. Comparative study in leg telangiectasias treatment with Nd:YAG laser and sclerotherapy // Exp Ther Med. 2019. Т. 17, № 2. С. 1106–1112.
- Lupton J.R., Alster T.S., Romero P. Clinical comparison of sclerotherapy versus long-pulsed Nd:YAG laser treatment for lower extremity telangiectases // Dermatol Surg. 2002. Т. 28, № 8. С. 694–697.
- Parlar B., Blazek C., Cazzaniga S., Naldi L., Kloetgen H.W., Borradori L., Buettiker U. Treatment of lower extremity telangiectasias in women by foam sclerotherapy vs. Nd:YAG laser: a prospective, comparative, randomized, open-label trial // J Eur Acad Dermatol Venereol. 2015. Т. 29, № 3. С. 549–554.
- IanoȘi N.G., Neagoe C.D., Tutunaru C.V., CĂlbureanu-Popescu M.X., DrĂguȘin L., GÎngeoveanu G., Farmazon A., PĂun I., IanoȘi S.L. Single Blind, Randomised Study Regarding the Treatment of the Telangiectasia of the Lower Limbs (C1EAP) Using Polidocanol 0,5%, 1%, and Nd:YAG Laser // Curr Health Sci J. 2020. Т. 46, № 2. С. 141–149.
- Cisneros J.L., Del Rio R., Palou J. Sclerosis and the Nd:YAG, Q-switched laser with multiple frequency for treatment of telangiectases, reticular veins, and residual pigmentation // Dermatol Surg. 1998. Т. 24, № 10. С. 1119–1123.
- Levy J.L., Elbahr C., Jouve E., Mordon S. Comparison and sequential study of long pulsed Nd:YAG 1,064 nm laser and sclerotherapy in leg telangiectasias treatment // Lasers Surg Med. 2004. Т. 34, № 3. С. 273–276.
- Moreno-Moraga J., Smarandache A., Pascu M.L., Royo J., Trelles M.A. 1064 nm Nd:YAG long pulse laser after polidocanol microfoam injection dramatically improves the result of leg vein treatment: a randomized controlled trial on 517 legs with a three-year follow-up // Phlebology. 2014. Т. 29, № 10. С. 658–666.
- Moreno-Moraga J., Pascu M.L., Alcolea J.M., Smarandache A., Royo J., David F., Trelles M.A. Effects of 1064-nm Nd:YAG long-pulse laser on polidocanol microfoam injected for varicose vein treatment: a controlled observational study of 404 legs, after 5-year-long treatment // Lasers Med Sci. 2019. Т. 34, № 7. С. 1325–1332.
- Bush R., Bush P. Evaluation of sodium tetradecyl sulfate and polidocanol as sclerosants for leg telangiectasia based on histological evaluation with clinical correlation // Phlebology. 2017. Т. 32, № 7. С. 496–500.
- Kahle B., Leng K. Efficacy of sclerotherapy in varicose veins-prospective, blinded, placebo-controlled study // Dermatol Surg. 2004. Т. 30, № 5. С. 723–728; discussion 728.
- Norris M.J., Carlin M.C., Ratz J.L. Treatment of essential telangiectasia: effects of increasing concentrations of polidocanol // J Am Acad Dermatol. 1989. Т. 20, № 4. С. 643–649.
- Rabe E., Schliephake D., Otto J., Breu F.X., Pannier F. Sclerotherapy of telangiectases and reticular veins: a double-blind, randomized, comparative clinical trial of polidocanol, sodium tetradecyl sulphate and isotonic saline (EASI study) // Phlebology. 2010. Т. 25, № 3. С. 124–131.
- Uncu H. Sclerotherapy: a study comparing polidocanol in foam and liquid form // Phlebology. 2010. Т. 25, № 1. С. 44–49.
- Peterson J.D., Goldman M.P., Weiss R.A., Duffy D.M., Fabi S.G., Weiss M.A., Guiha I. Treatment of reticular and telangiectatic leg veins: double-blind, prospective comparative trial of polidocanol and hypertonic saline // Dermatol Surg. 2012. Т. 38, № 8. С. 1322–1330.
- Kern P., Ramelet A.-A., Wütschert R., Hayoz D. Compression after sclerotherapy for telangiectasias and reticular leg veins: a randomized controlled study // J Vasc Surg. 2007. Т. 45, № 6. С. 1212–1216.
- Guidelines of care for sclerotherapy treatment of varicose and telangiectatic leg veins. American Academy of Dermatology // J Am Acad Dermatol. 1996. Т. 34, № 3. С. 523–528.
- Rabe E., Pannier-Fischer F., Gerlach H., Breu F.X., Guggenbichler S., Zabel M., German Society of Phlebology. Guidelines for sclerotherapy of varicose veins // Dermatol Surg. 2004. Т. 30, № 5. С. 687–693.
- Rabe E., Pannier F., Gerlach H., Breu F.X., Guggenbichler S., Wollmann J. Leitlinie Sklerosierungsbehandlung der Varikose // Phlebologie. 2008. Т. 37. С. 27–34.
- Guex J.-J. [Contra indications of sclerotherapy, update 2005] // J Mal Vasc. 2005. Т. 30, № 3. С. 144–149.
- Stücker M., Reich S., Hermes N., Altmeyer P. Safety and efficiency of perilesional sclerotherapy in leg ulcer patients with postthrombotic syndrome and/or oral anticoagulation with phenprocoumon // J Dtsch Dermatol Ges. J Dtsch Dermatol Ges, 2006. Т. 4, № 9. С. 734–738.
- Gachet G., Spini L. Scle´rothe´rapie des varices sous anticoagulants // Phlebologie. 2002. Т. 55. С. 41–44.
- Samama M.M. An epidemiologic study of risk factors for deep vein thrombosis in medical outpatients: the Sirius study // Arch Intern Med. 2000. Т. 160, № 22. С. 3415–3420.
- Cheng Y.-J., Liu Z.-H., Yao F.-J., Zeng W.-T., Zheng D.-D., Dong Y.-G., Wu S.-H. Current and former smoking and risk for venous thromboembolism: a systematic review and meta-analysis // PLoS Med. 2013. Т. 10, № 9. С. e1001515.
- Zhang G., Xu X., Su W., Xu Q. Smoking and risk of venous thromboembolism: a systematic review // Southeast Asian J Trop Med Public Health. 2014. Т. 45, № 3. С. 736–745.
- Rao J., Wildemore J.K., Goldman M.P. Double-blind prospective comparative trial between foamed and liquid polidocanol and sodium tetradecyl sulfate in the treatment of varicose and telangiectatic leg veins // Dermatol Surg. 2005. Т. 31, № 6. С. 631–635; discussion 635.
- Goldman M.P. Treatment of varicose and telangiectatic leg veins: double-blind prospective comparative trial between aethoxyskerol and sotradecol // Dermatol Surg. 2002. Т. 28, № 1. С. 52–55.
- Goldman M.P., Kaplan R.P., Oki L.N., Cavender P.A., Strick R.A., Bennett R.G. Sclerosing agents in the treatment of telangiectasia. Comparison of the clinical and histologic effects of intravascular polidocanol, sodium tetradecyl sulfate, and hypertonic saline in the dorsal rabbit ear vein model // Arch Dermatol. 1987. Т. 123, № 9. С. 1196–1201.
- Alòs J., Carreño P., López J.A., Estadella B., Serra-Prat M., Marinel-Lo J. Efficacy and safety of sclerotherapy using polidocanol foam: a controlled clinical trial // Eur J Vasc Endovasc Surg. 2006. Т. 31, № 1. С. 101–107.
- Bertanha M., Jaldin R.G., Moura R., Pimenta R.E.F., Mariúba J.V. de O., Lúcio Filho C.E.P., Alcantara G.P., Padovani C.R., Yoshida W.B., Sobreira M.L. Sclerotherapy for Reticular Veins in the Lower Limbs: A Triple-Blind Randomized Clinical Trial // JAMA Dermatol. 2017. Т. 153, № 12. С. 1249–1255.
- Bertanha M., Yoshida W.B., Bueno de Camargo P.A., Moura R., Reis de Paula D., Padovani C.R., Sobreira M.L. Polidocanol Plus Glucose Versus Glucose Alone for the Treatment of Telangiectasias: Triple Blind, Randomised Controlled Trial (PG3T) // Eur J Vasc Endovasc Surg. 2021. Т. 61, № 1. С. 128–135.
- Bukina O.V., Sinitsyn A.A., Efremova O.I., Pelevin A.V. Low concentration of sodium tetradecyl sulfate and hypertonic glucose solution for the treatment of telangiectasia: A prospective randomized clinical trial // Phlebology. 2023. Т. 38, № 9. С. 622–627.
- Bukina O.V., Sinitsyn A.A. Hypertonic Glucose in the Treatment of Telangiectatic Matting: a Pilot Study // Flebol. 2019. Т. 13, № 4. С. 314.
- Munia M.A., Wolosker N., Munia C.G., Chao W.S., Puech-Leão P. Comparison of laser versus sclerotherapy in the treatment of lower extremity telangiectases: a prospective study // Dermatol Surg. 2012. Т. 38, № 4. С. 635–639.
- Hoss E., Kollipara R., Boen M., Alhaddad M., Goldman M.P. Comparison of the Safety and Efficacy of Foam Sclerotherapy With 1: 2 Polidocanol to Air Ratio Versus 1: 4 Ratio for the Treatment of Reticular Veins of the Lower Extremities // Dermatol Surg. 2020. Т. 46, № 12. С. 1715–1720.
- Sadoun S., Benigni J., Sica M. Etude prospective de l0 efficacite´ de la mousse de scle´rosant dans le traitement des varices tronculaires des membres infe´rieurs // Phlebologie. 2002. Т. 55. С. 259–262.
- Tessari L., Cavezzi A., Frullini A. Preliminary experience with a new sclerosing foam in the treatment of varicose veins // Dermatol Surg. 2001. Т. 27, № 1. С. 58–60.
- de Roos K.-P., Groen L., Leenders A.C.A.P. Foam sclerotherapy: investigating the need for sterile air // Dermatol Surg. 2011. Т. 37, № 8. С. 1119–1124.
- Chen J., Liu Y.-R., Sun Y.-D., Liu C., Zhuo S.-Y., Li K., Wei F.-C., Liu S.-H. The risk of bacteria in foam sclerotherapy: does the condition of the air in outpatient vs. operating rooms make a difference? // Br J Dermatol. 2014. Т. 171, № 6. С. 1386–1390.
- Cavezzi A., Tessari L. Foam sclerotherapy techniques: different gases and methods of preparation, catheter versus direct injection // Phlebology. 2009. Т. 24, № 6. С. 247–251.
- Morrison N., Neuhardt D.L., Rogers C.R., McEown J., Morrison T., Johnson E., Salles-Cunha S.X. Comparisons of side effects using air and carbon dioxide foam for endovenous chemical ablation // J Vasc Surg. 2008. Т. 47, № 4. С. 830–836.
- Morrison N., Neuhardt D.L., Rogers C.R., McEown J., Morrison T., Johnson E., Salles-Cunha S.X. Incidence of side effects using carbon dioxide-oxygen foam for chemical ablation of superficial veins of the lower extremity // Eur J Vasc Endovasc Surg. 2010. Т. 40, № 3. С. 407–413.
- Beckitt T., Elstone A., Ashley S. Air versus physiological gas for ultrasound guided foam sclerotherapy treatment of varicose veins // Eur J Vasc Endovasc Surg. 2011. Т. 42, № 1. С. 115–119.
- Hesse G., Breu F., Kuschmann A., Hartmann K., Salomon N. Sclerotherapy using air- or CO 2-O 2-foam. Post-approval study // Phlebologie. 2012. Т. 41. С. 77–88.
- Parsi K. Paradoxical embolism, stroke and sclerotherapy // Phlebology. 2012. Т. 27, № 4. С. 147–167.
- Adatia S., Nambiar V., Kapadia R., Abuzinath A., Apel S., Alqarni M., Subramaniam S., Menon B. Acute ischemic stroke caused by paradoxical air embolism following injection sclerotherapy for varicose veins // Neurol India. 2013. Т. 61, № 4. С. 431–433.
- Tan M.K.H., Salim S., Onida S., Davies A.H. Postsclerotherapy compression: A systematic review // J Vasc Surg Venous Lymphat Disord. 2021. Т. 9, № 1. С. 264–274.
- Ra W., Ns S., Mp G., Ma W. Post-sclerotherapy compression: controlled comparative study of duration of compression and its effects on clinical outcome // Dermatologic surgery : official publication for American Society for Dermatologic Surgery [et al.]. Dermatol Surg, 1999. Т. 25, № 2.
- Nootheti P.K., Cadag K.M., Magpantay A., Goldman M.P. Efficacy of graduated compression stockings for an additional 3 weeks after sclerotherapy treatment of reticular and telangiectatic leg veins // Dermatol Surg. 2009. Т. 35, № 1. С. 53–57; discussion 57-58.
- Bayer A., Kuznik N., Langan E.A., Recke A., Recke A.-L., Faerber G., Kaschwich M., Kleemann M., Kahle B. Clinical outcome of short-term compression after sclerotherapy for telangiectatic varicose veins // J Vasc Surg Venous Lymphat Disord. 2021. Т. 9, № 2. С. 435–443.
- Feied C.F., Jackson J.J., Bren T.S., Bond O.B., Fernando C.E., Young V.C., Hashemiyoon R.B. Allergic reactions to polidocanol for vein sclerosis. Two case reports // J Dermatol Surg Oncol. 1994. Т. 20, № 7. С. 466–468.
- Pradalier A., Vincent D., Hentschel V., Cohen-Jonathan A.M., Daniel E. Allergie aux sclérosants des varices // Revue Française d’Allergologie et d’Immunologie Clinique. 1995. Т. 35, № 5. С. 440–443.
- Cavezzi A., Parsi K. Complications of foam sclerotherapy // Phlebology. 2012. Т. 27 Suppl 1. С. 46–51.
- Goldman M.P., Sadick N.S., Weiss R.A. Cutaneous necrosis, telangiectatic matting, and hyperpigmentation following sclerotherapy. Etiology, prevention, and treatment // Dermatol Surg. 1995. Т. 21, № 1. С. 19–29; quiz 31–32.
- Bergan J.J., Weiss R.A., Goldman M.P. Extensive tissue necrosis following high-concentration sclerotherapy for varicose veins // Dermatol Surg. 2000. Т. 26, № 6. С. 535–541; discussion 541-542.
- Bihari I., Magyar E null. Reasons for ulceration after injection treatment of telangiectasia // Dermatol Surg. 2001. Т. 27, № 2. С. 133–136.
- Schuller-Petrović S., Pavlović M.D., Neuhold N., Brunner F., Wölkart G. Subcutaneous injection of liquid and foamed polidocanol: extravasation is not responsible for skin necrosis during reticular and spider vein sclerotherapy // J Eur Acad Dermatol Venereol. 2011. Т. 25, № 8. С. 983–986.
- Geukens J., Rabe E., Bieber T. Embolia cutis medicamentosa of the foot after sclerotherapy // Eur J Dermatol. 1999. Т. 9, № 2. С. 132–133.
- Ramelet A.-A., Parmentier L. Delayed Nicolau’s livedoid dermatitis after ultrasound-guided sclerotherapy // Dermatol Surg. 2010. Т. 36, № 1. С. 155–158.
- Guex J.-J., Allaert F.-A., Gillet J.-L., Chleir F. Immediate and midterm complications of sclerotherapy: report of a prospective multicenter registry of 12,173 sclerotherapy sessions // Dermatol Surg. 2005. Т. 31, № 2. С. 123–128; discussion 128.
- Kern P., Ramelet A.-A., Wutschert R., Bounameaux H., Hayoz D. Single-blind, randomized study comparing chromated glycerin, polidocanol solution, and polidocanol foam for treatment of telangiectatic leg veins // Dermatol Surg. 2004. Т. 30, № 3. С. 367–372; discussion 372.
- Frullini A., Felice F., Burchielli S., Di Stefano R. High production of endothelin after foam sclerotherapy: a new pathogenetic hypothesis for neurological and visual disturbances after sclerotherapy // Phlebology. 2011. Т. 26, № 5. С. 203–208.
- Frullini A., Barsotti M.C., Santoni T., Duranti E., Burchielli S., Di Stefano R. Significant endothelin release in patients treated with foam sclerotherapy // Dermatol Surg. 2012. Т. 38, № 5. С. 741–747.
- Hamel-Desnos C.M., Desnos P.R., Ferre B., Le Querrec A. In vivo biological effects of foam sclerotherapy // Eur J Vasc Endovasc Surg. 2011. Т. 42, № 2. С. 238–245.
- Fabi S.G., Peterson J.D., Goldman M.P., Guiha I. An investigation of coagulation cascade activation and induction of fibrinolysis using foam sclerotherapy of reticular veins // Dermatol Surg. 2012. Т. 38, № 3. С. 367–372.
- Georgiev M. Postsclerotherapy hyperpigmentations: a one-year follow-up // J Dermatol Surg Oncol. 1990. Т. 16, № 7. С. 608–610.
- Scultetus A.H., Villavicencio J.L., Kao T.-C., Gillespie D.L., Ketron G.D., Iafrati M.D., Pikoulis E., Eifert S. Microthrombectomy reduces postsclerotherapy pigmentation: multicenter randomized trial // J Vasc Surg. 2003. Т. 38, № 5. С. 896–903.
- Munavalli G.S., Weiss R.A. Complications of sclerotherapy // Semin Cutan Med Surg. 2007. Т. 26, № 1. С. 22–28.
- Hill D.A. Neurological and chest symptoms following sclerotherapy: a single centre experience // Phlebology. 2014. Т. 29, № 9. С. 619–627.
- Gonzalez Ochoa A.J., Carrillo J., Manríquez D., Manrique F., Vazquez A.N. Reducing hyperpigmentation after sclerotherapy: A randomized clinical trial // J Vasc Surg Venous Lymphat Disord. 2021. Т. 9, № 1. С. 154–162.
- Bogachev V.Y., Boldin B.V., Turkin P.Y. Administration of Micronized Purified Flavonoid Fraction During Sclerotherapy of Reticular Veins and Telangiectasias: Results of the National, Multicenter, Observational Program VEIN ACT PROLONGED-C1 // Adv Ther. 2018. Т. 35, № 7. С. 1001–1008.
- Meesters A.A., Pitassi L.H.U., Campos V., Wolkerstorfer A., Dierickx C.C. Transcutaneous laser treatment of leg veins // Lasers Med Sci. 2014. Т. 29, № 2. С. 481–492.
- Guex J.-J. Complications of sclerotherapy: an update // Dermatol Surg. 2010. Т. 36 Suppl 2. С. 1056–1063.
- McCoppin H.H., Hovenic W.W., Wheeland R.G. Laser treatment of superficial leg veins: a review // Dermatol Surg. 2011. Т. 37, № 6. С. 729–741.
- Сэдик Н., Лоуренс Н., Мой Р., Хирш Р.Д. Косметическая хирургия кожи пер. с англ. // МЕДпресс-информ. 2009. С. 144.
- Navratil L., Kymplova J. Contraindications in noninvasive laser therapy: truth and fiction // J Clin Laser Med Surg. 2002. Т. 20, № 6. С. 341–343.
- Santana-Blank L. Contraindications in noninvasive laser therapy: truth and fiction // Photomed Laser Surg. 2004. Т. 22, № 5. С. 442; author reply 442.
- Fourtanier A., Moyal D., Seité S. Sunscreens containing the broad-spectrum UVA absorber, Mexoryl SX, prevent the cutaneous detrimental effects of UV exposure: a review of clinical study results // Photodermatol Photoimmunol Photomed. 2008. Т. 24, № 4. С. 164–174.
- Alam M., Warycha M. Complications of lasers and light treatments // Dermatol Ther. 2011. Т. 24, № 6. С. 571–580.
- Adamič M., Pavlović M.D., Troilius Rubin A., Palmetun-Ekbäck M., Boixeda P. Guidelines of care for vascular lasers and intense pulse light sources from the European Society for Laser Dermatology // J Eur Acad Dermatol Venereol. 2015. Т. 29, № 9. С. 1661–1678.
- Ef B., A N.-T., B R. Treatment of spider veins of the lower extremity with a novel 532 nm KTP laser // Lasers Surg Med. Lasers Surg Med, 2014. Т. 46, № 2.
- Fournier N., Brisot D., Mordon S. Treatment of leg telangiectases with a 532 nm KTP laser in multipulse mode // Dermatol Surg. 2002. Т. 28, № 7. С. 564–571.
- Woo W.K., Jasim Z.F., Handley J.M. 532-nm Nd:YAG and 595-nm pulsed dye laser treatment of leg telangiectasia using ultralong pulse duration // Dermatol Surg. 2003. Т. 29, № 12. С. 1176–1180; discussion 1180.
- Bernstein E.F. The new-generation, high-energy, 595 nm, long pulse-duration, pulsed-dye laser effectively removes spider veins of the lower extremity // Lasers Surg Med. 2007. Т. 39, № 3. С. 218–224.
- Kono T., Yamaki T., Erçöçen A.R., Fujiwara O., Nozaki M. Treatment of leg veins with the long pulse dye laser using variable pulse durations and energy fluences // Lasers Surg Med. 2004. Т. 35, № 1. С. 62–67.
- Bäumler W., Ulrich H., Hartl A., Landthaler M., Shafirstein G. Optimal parameters for the treatment of leg veins using Nd:YAG lasers at 1064 nm // Br J Dermatol. 2006. Т. 155, № 2. С. 364–371.
- Trelles M.A., Allones I., Martín-Vázquez M.J., Trelles O., Vélez M., Mordon S. Long pulse Nd:YAG laser for treatment of leg veins in 40 patients with assessments at 6 and 12 months // Lasers Surg Med. 2004. Т. 35, № 1. С. 68–76.
- Ozden M.G., Bahçivan M., Aydin F., Şentürk N., Bek Y., Cantürk T., Turanli A.Y. Clinical comparison of potassium-titanyl-phosphate (KTP) versus neodymium:YAG (Nd:YAG) laser treatment for lower extremity telangiectases // J Dermatolog Treat. 2011. Т. 22, № 3. С. 162–166.
- Ross E.V., Meehan K.J., Gilbert S., Domankevitz Y. Optimal pulse durations for the treatment of leg telangiectasias with an alexandrite laser // Lasers Surg Med. 2009. Т. 41, № 2. С. 104–109.
- Trelles M.A., Allones I., Alvarez J., Vélez M., Martín-Vázquez M., Trelles O.R., Luna R., Buil C., Mordon S.R. The 800-nm diode laser in the treatment of leg veins: assessment at 6 months // J Am Acad Dermatol. 2006. Т. 54, № 2. С. 282–289.
- Eremia S., Li C., Umar S.H. A side-by-side comparative study of 1064 nm Nd:YAG, 810 nm diode and 755 nm alexandrite lasers for treatment of 0.3-3 mm leg veins // Dermatol Surg. 2002. Т. 28, № 3. С. 224–230.
- Passeron T., Olivier V., Duteil L., Desruelles F., Fontas E., Ortonne J.-P. The new 940-nanometer diode laser: an effective treatment for leg venulectasia // J Am Acad Dermatol. 2003. Т. 48, № 5. С. 768–774.
- Anderson R.R., Parrish J.A. The optics of human skin // J Invest Dermatol. 1981. Т. 77, № 1. С. 13–19.
- Ross E.V., Domankevitz Y. Laser treatment of leg veins: Physical mechanisms and theoretical considerations // Lasers Surg Med. 2005. Т. 36, № 2. С. 105–116.
- Anderson R.R., Parrish J.A. Selective photothermolysis: precise microsurgery by selective absorption of pulsed radiation // Science. 1983. Т. 220, № 4596. С. 524–527.
- Tanzi E.L., Lupton J.R., Alster T.S. Lasers in dermatology: four decades of progress // J Am Acad Dermatol. 2003. Т. 49, № 1. С. 1–31; quiz 31–34.
- Parlette E.C., Groff W.F., Kinshella M.J., Domankevitz Y., O’Neill J., Ross E.V. Optimal pulse durations for the treatment of leg telangiectasias with a neodymium YAG laser // Lasers Surg Med. 2006. Т. 38, № 2. С. 98–105.
- Garden J.M., Tan O.T., Kerschmann R., Boll J., Furumoto H., Anderson R.R., Parrish J.A. Effect of dye laser pulse duration on selective cutaneous vascular injury // J Invest Dermatol. 1986. Т. 87, № 5. С. 653–657.
- Dierickx C.C., Casparian J.M., Venugopalan V., Farinelli W.A., Anderson R.R. Thermal relaxation of port-wine stain vessels probed in vivo: the need for 1-10-millisecond laser pulse treatment // J Invest Dermatol. 1995. Т. 105, № 5. С. 709–714.
- Anderson R.R., Parrish J.A. Microvasculature can be selectively damaged using dye lasers: a basic theory and experimental evidence in human skin // Lasers Surg Med. 1981. Т. 1, № 3. С. 263–276.
- Hohenleutner U., Walther T., Wenig M., Bäumler W., Landthaler M. Leg telangiectasia treatment with a 1.5 ms pulsed dye laser, ice cube cooling of the skin and 595 vs 600 nm: preliminary results // Lasers Surg Med. 1998. Т. 23, № 2. С. 72–78.
- Buscher B.A., McMeekin T.O., Goodwin D. Treatment of leg telangiectasia by using a long-pulse dye laser at 595 nm with and without dynamic cooling device // Lasers Surg Med. 2000. Т. 27, № 2. С. 171–175.
- Tanghetti E., Sherr E. Treatment of telangiectasia using the multi-pass technique with the extended pulse width, pulsed dye laser (Cynosure V-Star) // J Cosmet Laser Ther. 2003. Т. 5, № 2. С. 71–75.
- Eremia S., Li C.Y. Treatment of leg and face veins with a cryogen spray variable pulse width 1064-nm Nd:YAG laser--a prospective study of 47 patients // J Cosmet Laser Ther. 2001. Т. 3, № 3. С. 147–153.
- Nanni. Handling complications of laser treatment. // Dermatol Ther. 2000. Т. 13. С. 127–139.
- Boixeda P., Núñez M., Pérez B., de las Heras M.E., Hilara Y., Ledo A. Complications of 585-nm pulsed dye laser therapy // Int J Dermatol. 1997. Т. 36, № 5. С. 393–397.
- Hammes S., Kimmig W. [Side effects and complications of therapy with laser and intense light sources] // Hautarzt. 2013. Т. 64, № 3. С. 145–154.
- Hirsch R. Iatrogenic laser complications // Clin Dermatol. 2011. Т. 29, № 6. С. 691–695.
- Alster T.S., Khoury R.R. Treatment of laser complications // Facial Plast Surg. 2009. Т. 25, № 5. С. 316–323.
- Willey A., Anderson R.R., Azpiazu J.L., Bakus A.D., Barlow R.J., Dover J.S., Garden J.M., Kilmer S.L., Landa N., Manstein D., Ross E.V., Sadick N., Tanghetti E.A., Yaghmai D., Zelickson B.D. Complications of laser dermatologic surgery // Lasers Surg Med. 2006. Т. 38, № 1. С. 1–15.
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
состав группы будет внесен после завершения работы над рекомендациями
Все члены Рабочей группы подтвердили отсутствие финансовой поддержки или другого конфликта интересов при составлении данных рекомендаций.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория разработанных клинических рекомендаций:
- Врач – сердечно-сосудистый хирург;
- Врач – хирург;
- Врач – косметолог;
- Врач - ультразвуковой диагностики;
- Студенты медицинских ВУЗов, ординаторы, аспиранты.
Рекомендации основаны на совокупном анализе доказательств, представленных в мировой литературе и полученных в результате клинического применения современных принципов и методов диагностики и лечения других уточненных поражений вен конечностей (ретикулярные вены и телеангиэктазии). Основные положения Рекомендаций ранжируются в соответствии с Приказом Министерства здравоохранения РФ от 28 февраля 2019 г. № 103н "Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации”. Рекомендации подготовлены в соответствии с Методическими рекомендациями по проведению оценки научной обоснованности включаемой в клинические рекомендации информации, ФГБУ «Центр экспертизы и контроля качества медицинской помощи» Министерства здравоохранения Российской Федерации, 2019 г.
- Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств):
- Систематические обзоры исследований с контролем референтным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа
- Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
- Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования
- Несравнительные исследования, описание клинического случая
- Имеется лишь обоснование механизма действия или мнение экспертов
- Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации:
- Систематический обзор рандомизированных клинических исследований с применением мета-анализа
- Отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа
- Нерандомизированные сравнительные исследования, в том числе когортные исследования
- Несравнительные исследования, описание клинического случая или серии случаев, исследование «случай-контроль»
- Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов
- Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
- Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными)
- Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными)
- Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными)
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
- Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации»;
- Приказ Минздрава России от 15.11.2012 № 918н «Об утверждении Порядка оказания медицинской помощи больным с сердечно-сосудистыми заболеваниями»;
- Приказ Минздрава России от 15.11.2012 № 922н «Об утверждении Порядка оказания медицинской помощи взрослому населению по профилю «хирургия»;
- Приказ Минздрава России от 7 июля 2015 г. N 422 ан "Об утверждении критериев оценки качества медицинской помощи";
- Письмо ФСС РФ от 01.09.2000 N 02-18/10-5766 "Об ориентировочных сроках временной нетрудоспособности при наиболее распространенных заболеваниях и травмах";
- Постановление Правительства РФ от 20.02.2006 N 95 (ред. от 10.08.2016) "О порядке и условиях признания лица инвалидом";
- Приказ Министерства Здравоохранения и Социального развития Российской Федерации от 17 декабря 2015 г. № 1024н «О классификации и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы».
- Приказ Министерства здравоохранения РФ от 28 февраля 2019 г. № 103н "Об утверждении порядка и сроков разработки клинических рекомендаций, их пересмотра, типовой формы клинических рекомендаций и требований к их структуре, составу и научной обоснованности включаемой в клинические рекомендации информации”.
- Инструкция по медицинскому применению препарата Этоксисклерол, международное непатентованное название: Лауромакрогол-400, Минздрав России П№11397/01-140109
- Инструкция по медицинскому применению препарата Фибро-Вейн (FIBRO-VEIN), международное непатентованное название: натрия тетрадецилсульфат, Минздрав России П№014787/01-181212
Приложение Б. Алгоритмы действий врача
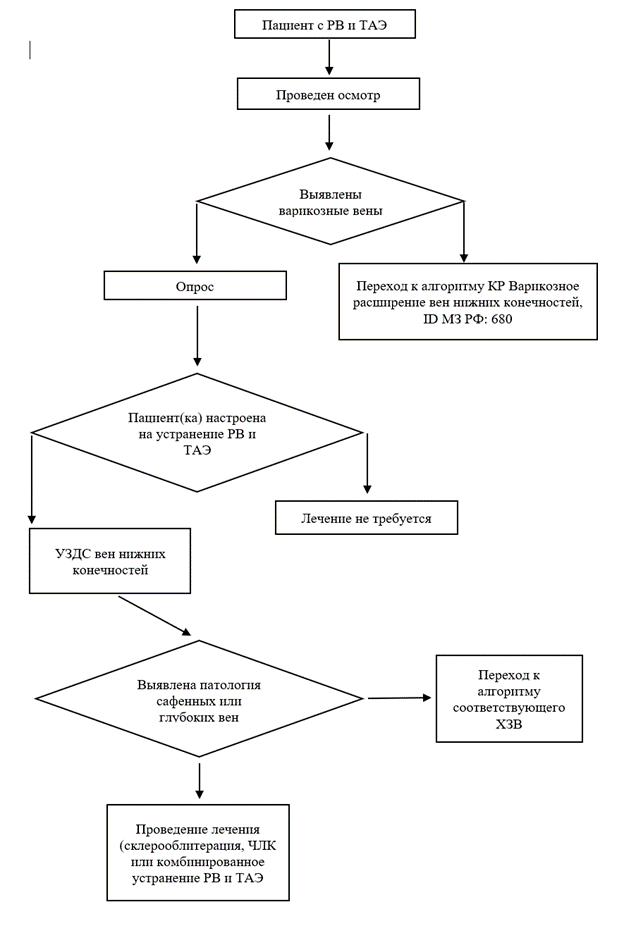
Приложение В. Информация для пациентов
Ретикулярные вены и телеангиоэктазии нижних конечностей относятся к хроническим медленно прогрессирующим заболеваниям вен нижних конечностей, в основе которых лежит наследственно и гормонально обусловленная слабость венозной стенки. В то же время это заболевание не относится к генетическим. Для возникновения ретикулярных вен и телеангиоэктазий нижних конечностей важную роль играют: пол, прием гормональных контрацептивов и общее старение кожи.
Чаще всего наличие ретикулярных вен и телеангиоэктазий не сопровождаются симптомами и носят сугубо эстетический недостаток.
Данное заболевание, в отличие от варикозной болезни, не приводит к развитию тромботических и трофических осложнений.
Диагноз - ретикулярные вены и телеангиоэктазии нижних конечностей устанавливается врачом после клинического осмотра и не требует подтверждения выполнением ультразвукового сканирования вен.
Основная цель устранения или уменьшения количества ретикулярных вен и телеангиоэктазий нижних конечностей – эстетическая, улучшение внешнего вида ноги.
Основными методами лечения данной патологии являются: склеротерапия и чрескожная лазерная коагуляция, а также комбинация этих методов.
Cклеротерапия (флебосклерозирование, склерооблитерация) - метод удаления варикозных вен, заключающийся в инъекционном (с помощью шприца и иглы) введении в их просвет специальных препаратов-склерозантов.
Флебосклерозирующие препараты (или склерозанты - специально разработанные вещества на основе спиртов) предназначенные для внутривенного введения. Склерозанты вызывают разрушение внутреннего (эндотелиального) слоя вены и ее значительное сужение, что создает условия для склерооблитерации (склеивания) и полного закрытия венозного сосуда. Препарат, его концентрация и объем подбираются врачом индивидуально для каждого пациента. При правильном использовании склерозант вызывает только местное действие и его общее токсическое воздействие на организм исключено. При попадании небольшого количества склерозанта в глубокую венозную систему происходит его быстрое растворение (кровоток в глубоких венах намного выше, чем в поверхностных) без местного и общего повреждающего действия. Сразу после воздействия склерозанта в просвете вены формируется специфический сгусток («склеротромб», «коагула»), в результате чего сосуд становится плотным, слегка болезненным. Далее начинается процесс рассасывания вены, который может занимать 2 - 6 месяцев, в течение которых происходит формирование тонкого соединительнотканного тяжа и его практически полное исчезновение через 1 - 1,5 года. Обычно сеансы склеротерапии проводятся один раз в неделю. Продолжительность лечения зависит от стадии и формы заболевания и определяется лечащим врачом. Положительный косметический результат лечения проявляется не ранее, чем через 2 - 8 недель после окончания склеротерапии.
Для устранения реткулярных вен и телеангиэктазий могут применяться различные разновидности склеротерапии и их комбинация: склеротерапия жидкой и пенной формой склерозанта, Вид и способ склеротерапии определяет лечащий врач. Процедура склеротерапии заключается в пункции вены иглой различного диаметра, что зависит от калибра сосуда, и внутрисосудистом введении препарата. Процедура может быть слегка болезненной, но специального обезболивания не требует. Во время введения препарата могут наблюдаться ощущения покалывания, жжения по ходу вены. Количество инъекцией на один сеанс определяется индивидуально, исходя из степени поражения и максимально допустимого количества препарата.
В периоде подготовки к склеротерапии и после ее выполнения следует помнить простые правила:
- Склеротерапия является безопасным методом лечения с минимальным количеством противопоказаний, поэтому, подготовка к ней обычно не подразумевает проведения дополнительных методов обследования. Однако, в ряде случаев лечащему врачу может потребоваться дополнительная информация о состоянии Вашего здоровья, и он может назначить ряд лабораторных и инструментальных тестов.
- Пенная склеротерапия опасна для лиц с наличием врожденных пороков сердца, сопровождающихся шунтированием крови «справа-налево» (например, открытое овальное окно в межпредсердной перегородке). Если вы имеете подтвержденный порок сердца или ранее при проведении склеротерапии отмечали появление неврологических симптомов (двоение в глазах, выпадение полей зрения, нарушения речи, мигрене-подобные головные боли) в обязательном порядке предупредите об этом Вашего лежащего врача. Подобные явления не обязательно являются противопоказанием к повторной склеротерапии, но должны быть приняты лечащим врачом во внимание.
- Если Вы принимаете антикоагулянты или антитромбоцитарные препараты, обязательно предупредите об этом лежащего врача.
- Сразу после проведения процедуры на Вашу ногу будет наложен бандаж из эластичных бинтов и/или надет медицинский компрессионный трикотаж. В зависимости от формы поражения и вида склеротерапии Вам будет необходимо использовать компрессию в круглосуточном или ежедневном режиме на протяжении установленного времени. Уточните у своего лечащего врача режим эластичной компрессии (когда можно первый раз снимать бинт или чулок и мыть ногу, как долго необходимо спать в компрессии и на протяжении какого срока использовать ее непрерывно) и строго следуйте его предписаниям.
- Сразу после процедуры Вам будет рекомендована пешая прогулка на протяжении 30-40 минут. Уделите этой прогулке должное внимание, т.к. она необходима для полноценной эвакуации препарата из глубоких вен и для предотвращения образования в них тромбов. Во время прогулки следует полноценно сгибать ногу в коленном и голеностопном суставах и сокращать икроножную мышцу.
- В редких случаях у пациентов с большим объемом телеангиоэктазий и ретикулярных вен в первые сутки после склеротерапии появляется чувство легкого недомогания и/или головокружения, повышается температура тела до 37—38 °С. Эти изменения самочувствия быстро проходят после приема нестероидных противовоспалительных препаратов (например, ацетилсалициловая кислота**, ибупрофен**). При головокружении необходимо несколько минут посидеть или полежать. Обо всех изменениях самочувствия на время прохождения курса склеротерапии необходимо информировать Вашего лежащего врача.
- В первый раз после снятия компрессионного бандажа или медицинского трикотажа Вы можете обнаружить кровоизлияния в области выполненных инъекций, потемнение кожи, наличие припухших и болезненных вен. Данные реакции являются типичным последствием склеротерапии, поэтому не стоит их опасаться.
- Уплотнения, легкая болезненность, потемнение кожи по ходу ретикулярных вен могут сохраняться на протяжении нескольких месяцев.
- Если у Вас сухая кожа или появилось ее раздражение от эластических бинтов, нужно смазать кожу ног после мытья любым, удобные для Вас питательным кремом.
- Если у Вас появляется отек в области голеностопного сустава или болевые ощущения, чувство «распирания» в ноге (в первые сутки после сеанса склеротерапии), то необходимо снять бинт, расправить все складки бинта и, если это рекомендовано лечащим врачом, полностью перебинтовать ногу, но не ранее чем через 2 часа после сеанса. Далее, желательно пройтись в течение 30–40 минут. При использовании медицинского компрессионного трикотажа подобные ситуации возникают редко.
- Компрессионные изделия необходимо регулярно менять. Частота их смены определяется производителем, поэтому следуйте в этом вопросе официальной инструкции. При круглосуточном использовании трикотажа удобно иметь два комплекса компрессионных изделий.
- На весь период лечения лечащим врачом могут быть не рекомендованы горячие ванны, бани, сауны, любые другие тепловые и солнечные процедуры (включая солярий), а также "разогревающие" мази, компрессы; массаж ног; силовую физическую нагрузку (тренажеры с отягощениями); подъем тяжестей, ношение тяжелых сумок. Отнеситесь к этим ограничениям с вниманием.
- Для уменьшения выраженности побочных реакций склеротерапии Вам может быть рекомендован прием флеботропных лекарственных средств в стандартных дозировках в период выполнения склеротерапии.
- Необходимость снимать компрессионный бандаж или медицинский трикотаж перед проведением очередного сеанса склеротерапии уточните у своего лечащего врача.
- При проведении склеротерапии может возникать ряд нежелательных реакций и осложнений: аллергические реакции (чрезвычайно редко), глубокие некрозы кожи (чрезвычайно редко), поверхностные некрозы кожи (редко), гиперпигментация (часто), вторичные телеангиоэктазии (часто), повреждение нервов (чрезвычайно редко), дыхательные нарушения: затруднение вдоха, тяжесть за грудиной, кашель, чувство саднения, жжения в дыхательных путях (часто), неврологические нарушения: мигрене-подобные боли, нарушения зрения, речи (редко), транзиторные ишемические атаки и нарушения мозгового кровообращения (чрезвычайно редко), флебит подкожных вен (редко), симптоматический тромбоз глубоких вен и легочная эмболия (очень редко). О риске возникновения осложнений и их последствиях проконсультируйтесь у своего лечащего врача перед началом лечения.
Чрескожная лазерная коагуляция один из методов устранения сосудистых сеток (ТАЭ) и ретикулярных вен на ногах и лице.
Чрескожная лазерная коагуляция может быть рекомендована, как альтернатива склеротерапии, особенно у пациентов с фобией к инъекциям, при непереносимости склерозантов, при телеангиэктазиях, устойчивых к склеротерапии, при вторичных телеангиэктазиях (matting), при выраженной гиперпигментации на склеротерапию в анамнезе, при малом диаметре ТАЭ.
Существуют следующие противопоказания к чрескожной лазерной коагуляции при лечении пациентов с ретикулярными венами и телеангиэктазиями: фотодерматозы, порфирия, фотосенсебилизация, загар (2-4 недели до начала лечения), солнечные ожоги, активная вирусная или бактериальная инфекция, острый венозный тромбоз, беременность, активный онкологический процесс, эпилепсия, гипопигментация (витилиго), келоидные рубцы, холодовая аллергия, хроническая артериальная недостаточность, хронические кожные заболевания в стадии обострения.
В течение нескольких недель после ЧЛК происходит постепенное исчезновение коагулированных сосудов. Окончательный результат может быть оценен через несколько недель и даже месяцев после процедуры. В эти сроки возможно проведение повторной процедуры при недостаточном эффекте. Может потребоваться от 1 до 5 (в среднем 2–3) процедур в зависимости от каждого конкретного случая.
Сразу после процедуры можно вернуться к обычному образу жизни, включая работу. В первые сутки после процедуры не следует заниматься спортом. В течение 2-х недель после процедуры не следует принимать горячие ванны, делать массаж ног, применять грубые скрабы и пилинги. В течение 2-х недель не следует посещать сауну или баню, принимать солнечные ванны или посещать солярий, при необходимости использовать солнцезащитный крем SPF 50. Возможно легкое покраснение, отечность в течение нескольких суток, синяки, кровоподтеки в месте воздействия
К побочным эффектам и осложнениям чрескожной лазерной коагуляции ретикулярных вен и телеангиэктазий относятся: временная или постоянная гиперпигментация, вторичные телеангиэктазии, гипопигментации, экхимозы, отек и ожоги кожи, рубцевание кожи, реактивация герпетической инфекции, боль во время процедуры, низкая эффективность лечения, вторичные телеангиэктазии – появление новых сосудистых сеток. При существенном изменении моего самочувствия или состояния (выраженный болевой синдром, отек, кровотечение из зоны вмешательства, гематома, выраженное покраснение, приступ одышки, резкое падение артериального давления, приступ потери сознания, выраженное учащенное сердцебиение, появление пузырей, ранок или темных корок на коже и т.д.), следует незамедлительно обратиться в к своему лечащему врачу, а при невозможности в иную медицинскую организацию для дополнительного обследования и консультации с врачами-специалистами.
Приложение Г1-ГN Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Приложение Г1. Классификация фотопипа кожи Фитцпатрика
- I тип Кельтский. Люди этого фототипа имеют самый светлый оттенок кожи. Они практически никогда не загорают (их кожа не принимает загар), риск возникновения солнечных ожогов (обгорания) очень велик.
- II тип Нордический. Кожа этого типа также характеризуется светлым оттенком и высокой чувствительностью к УФ-излучению. Риск обгорания велик, как и в предыдущем случае. Однако нордический фототип кожи незначительно, но принимает загар.
- III тип Тёмный европейский. Фототип, характеризующийся светлым оттенком и минимальным обгоранием на солнце. Кожа хорошо поддается загару.
- IV тип Средиземноморский. Светло-коричневый оттенок кожи. Шанс солнечного ожога – минимальный. Загар на кожу ложится всегда хорошо.
- V тип Индонезийский. Коричневый оттенок кожи. Люди с этим фототипом кожи практически никогда не обгорают на солнце. Загар характеризуется тёмным оттенком.
- VI тип Африканский. Люди этого фототипа имеют наиболее тёмный оттенок кожи. Шанс обгорания на солнце практически нулевой. Загар лишь делает кожу ещё темнее.
Содержание
- Ретикулярные вены и телеангиэктазии нижних конечностей. Клинические рекомендации
- Текст в pdf
- Список сокращений
- Термины и определения
- 1. Краткая информация по заболеванию или состоянию (группе заболеваний или состояний)
- 1.0. Определение заболевания или состояния (группы заболеваний или состояний)
- 1.1. Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
- 1.2. Эпидемиоогия заболевания или состояния (группы заболеваний или состояний)
- 1.3. Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
- 1.4. Классификация заболевания или состояния (группы заболеваний или состояний)
- 1.5. Клиническая картина заболевания и состояния (группы заболеваний или состояний)
- 2. Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
- 2.0. Критерии установления диагноза (состояния)
- 2.1. Жалобы и анамнез
- 2.2. Физикальное обследование
- 2.3. Лабораторные диагностические исследования
- 2.4. Инструментальные диагностические исследования
- 2.5. Иные диагностические исследования
- 2.6. Критерии установления заболевания или состояния (группы заболеваний или состояний)
- 3. Лечение, включая медикаментозную и немедикаментозную терапию, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
- 3.0. Общие положения и тактика лечения
- 3.1. Склеротерапия
- 3.2. Чрескожная лазерная коагуляция
- 3.2.1. Показания к чрескожной лазерной коагуляции
- 3.2.2. Противопоказания к чрескожной лазерной коагуляции
- 3.2.3. Подготовка к чрескожной лазерной коагуляции
- 3.2.4. Выбор длины волны лазерного аппарата
- 3.2.5. Параметры чрескожной лазерной коагуляции
- 3.2.6. Побочные эффекты и осложнения
- 3.2.7. Правила безопасности при работе с лазерами
- 3.3. Комбинированное лечение
- 4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- 5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- 6. Организация оказания медицинской помощи
- 7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
- Критерии оказания качества медицинской помощи
- Список литературы
- Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
- Приложение А2. Методология разработки клинических рекомендаций
- Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов инструкции по применению лекарственного препарата
- Приложение Б. Алгоритмы действий врача
- Приложение В. Информация для пациентов
- Приложение Г1-ГN Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях